Алкены
Характеристики и физические свойства алкенов
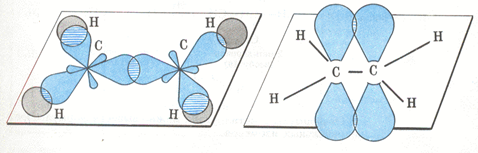
Рис. 1. Строение молекулы этилена.
По физическим свойствам алкены мало отличаются от алканов с тем же числом атомов углерода в молекуле. Низшие гомологи С2 – С4 при нормальных условиях – газы; С5 – С17 – жидкости; высшие гомологи – твердые вещества. Алкены нерастворимы в воде. Хорошо растворимы в органических растворителях.
Получение алкенов
В промышленности алкены получают при переработке нефти: крекингом и дегидрированием алканов. Лабораторные способы получения алкенов мы разделили на две группы:
- Реакции элиминирования (отщепления)
— дегидратация спиртов
CH3-CH2-OH → CH2=CH2 + H2O (H2SO4 (conc), t0 = 170).
— дегидрогалогенированиемоногалогеналканов
CH3-CH(Br)-CH2-CH3 + NaOHalcohol→ CH3-CH=CH-CH3 + NaBr + H2O (t0).
— дегалогенированиедигалогеналканов
CH3-CH(Cl)-CH(Cl)-CH2-CH3 + Zn(Mg) → CH3-CH=CH-CH2-CH3 + ZnCl2(MgCl2).
- Неполное гидрирование алкинов
CH≡CH + H2→CH2=CH2 (Pd, t0).
Химические свойства алкенов
Алкены – весьма реакционноспособоные органические соединения. Это объясняется их строением. Химия алкенов – это химия двойной связи. Типичные реакции для алкенов – реакции электрофильного присоединения.
Химические превращения алкенов протекают с расщеплением:
1) π-связи С-С (присоединение, полимеризация и окисление)
— гидрирование
CH3-CH=CH2 + H2→ CH3-CH2-CH2 (kat = Pt).
— галогенирование
CH3-CH2-CH=CH2 + Br2→ CH3-CH2-CH(Br)-CH2Br.
— гидрогалогенирование (протекает по правилу Марковникова: атом водорода присоединяется преимущественно к более гидрированному атому углерода)
CH3-CH=CH2 + H-Cl → CH3-CH(Cl)-CH3.
— гидратация
CH2=CH2 + H-OH → CH3-CH2-OH (H+, t0).
— полимеризация
nCH2=CH2→ -[-CH2-CH2-]-n (kat, t0).
— окисление
CH2=CH2 + 2KMnO4 + 2KOH → HO-CH2-CH2-OH + 2K2MnO4;
2CH2=CH2 + O2 → 2C2OH4 (эпоксид) (kat = Ag,t0);
2CH2=CH2 + O2 → 2CH3-C(O)H (kat = PdCl2, CuCl).
2) σ- и π-связей С-С
CH3-CH=CH-CH2-CH3 + 4[O] → CH3COOH + CH3CH2COOH (KMnO4, H+, t0).
3) связей Сsp3-Н (в аллильном положении)
CH2=CH2 + Cl2→ CH2=CH-Cl + HCl (t0=400).
4) Разрыв всех связей
C2H4 + 2O2→ 2CO2 + 2H2O;
CnH2n + 3n/2 O2→ nCO2 + nH2O.
Применение алкенов
Алкены нашли применение в различных отраслях народного хозяйства. Рассмотрим на примере отдельных представителей.
Этилен широко используется в промышленном органическом синтезе для получения разнообразных органических соединений, таких как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. В большом количестве этилен расходуется для производства полимеров.
Пропилен используется как сырье для получения некоторых спиртов (например, пропанола-2, глицерина), ацетона и др. Полимеризацией пропилена получают полипропилен.
Примеры решения задач
| Задание | При гидролизе водным раствором гидроксида натрия NaOH дихлорида, полученного присоединением 6,72 л хлора к этиленовому углеводороду, образовалось 22,8 г двухатомного спирта. Какова формула алкена, если известно, что реакции протекают с количественными выходами (без потерь)? |
| Решение | Запишем уравнение хлорирования алкена в общем виде, а также реакцию получения двухатомного спирта:
CnH2n + Cl2 = CnH2nCl2 (1); CnH2nCl2 + 2NaOH = CnH2n(OH)2 + 2HCl (2). Рассчитаем количество вещества хлора: n = V / Vm; n(Cl2) = V(Cl2) / Vm; n(Cl2) = 6,72 / 22,4 = 0,3 моль, следовательно, дихлорида этилена тоже будет 0,3 моль (уравнение 1), двухатомного спирта также должно получиться 0,3 моль, а по условию задачи это 22,8 г. Значит молярная масса его будет равна: M = m / n; M(CnH2n(OH)2) = m(CnH2n(OH)2) / n(CnH2n(OH)2); M(CnH2n(OH)2) = 22,8 / 0,3 = 76 г/моль. Найдем молярную массу алкена: M(CnH2n) = 76 – (2×17) = 42 г/моль, что соответствует формуле C3H6. |
| Ответ | Формула алкенаC3H6 |
| Задание | Сколько граммов потребуется для бромирования 16,8 г алкена, если известно, что при каталитическом гидрировании такого же количества алкена присоединилось 6,72 л водорода? Каков состав и возможное строение исходного углеводорода? |
| Решение | Запишем в общем виде уравнения бромирования и гидрирования алкена:
CnH2n + Br2 = CnH2nBr2 (1); CnH2n + H2 = CnH2n+2 (2). Рассчитаем количество вещества водорода: n = V / Vm; n(H2) = V(H2) / Vm; n(H2) = 6,72 / 22,4 = 0,3 моль, следовательно, алкена тоже будет 0,3 моль (уравнение 2), а по условию задачи это 16,8 г. Значит молярная масса его будет равна: M = m / n; M(CnH2n) = m(CnH2n) / n(CnH2n); M(CnH2n) = 16,8 / 0,3 = 56 г/моль, что соответствует формуле C4H8. Согласно уравнению (1) n(CnH2n) :n(Br2) = 1:1, т.е. n(Br2) = n(CnH2n) = 0,3 моль. Найдем массу брома: m = n×M; m(Br2) = n(Br2) × M(Br2); M(Br2) = 2×Ar(Br) = 2×80 = 160 г/моль; m(MnO2) = 0,3 × 160 = 48 г. Составим структурные формулы изомеров: бутен-1 (1), бутен-2 (2), 2-метилпропен (3), циклобутан (4). CH2=CH-CH2-CH3 (1); CH3-CH=CH-CH3 (2); CH2=C(CH3)-CH3 (3); C4H8 (4). |
| Ответ | Масса брома равна 48 г |











