Плотность толуола
Плотность толуола и другие его физические свойства
Горюч, сгорает коптящим пламенем. Обладает резким запахом, а также слабовыраженным наркотическим действием. Основные физические константы толуола приведены в табл. 1. Применяется в производстве взрывчатых веществ, бензойной кислоты, сахарина, лаков, типографских красок. Он употребляется в качестве добавки к моторному топливу как компонент высокооктановых бензинов.
Таблица 1. Физические свойства и плотность толуола.
|
Плотность, г/см3 |
0,86694 |
|
Температура плавления, oС |
-95 |
|
Температура кипения, oС |
110,6 |
|
Удельная теплота испарения, кДж/кг |
364 |
Толуол на два порядка менее токсичен, чем бензол, вследствие того что окисляется в бензойную кислоту и экскретируется из организма. Во всех случаях, где это возможно, следует производить замену бензола на толуол.
Химический состав и строение молекулы толуола
Химический состав молекулы толуола можно отразить с помощью эмпирической формулы C6H5-CH3. Радикал метил непосредственно связан с бензольным кольцом 7 Структурная формула толуола выглядит следующим образом:
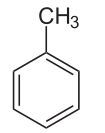
Рис. 1. Строение молекулы толуола.
Краткое описание химических свойств и плотность толуола
Для толуола, как и для всех ароматических углеводородов характерны реакции замещения в бензольном кольце, которые протекают по электрофильному механизму. За счет наличия в составе толуола радикала метила, замещение атомов водорода чаще всего происходит в орто- или пара-положении:
-галогенирование (толуол взаимодействует с хлором и бромом в присутствии катализаторов – безводных AlCl3, FeCl3, AlBr3)
C6H5-CH3 + Cl2 = C6H4Cl-CH3 + HCl;
— нитрование (толуол легко реагирует с нитрующей смесью – смесь концентрированных азотной и серной кислот)
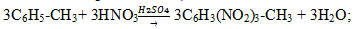
— алкилирование по Фридею-Крафтсу
C6H5-CH3+ CH3-CH(CH3)-Cl = CH3-C6H4-CH(CH3)-CH3 + HCl.
Реакции присоединения к толуолу приводят к разрушению ароматической системы и протекают только в жестких условиях:
— гидрирование (реакция протекает при нагревании, катализатор – Pt)
C6H5-CH3 + 3H2 = C6H11-CH3.
В результате окисления толуола образуется бензойная кислота:
5C6H5-CH3 + 6KMnO4 + 9H2SO4 = 5C6H5COOH + 6MnSO4 + 3K2SO4 + 14H2O;
Реакция взаимодействия толуола с хлором на свету приводит к замещению в углеводородном радикале:
C6H5-CH3 + Cl2 = C6H5-CH2Cl + HCl.
Примеры решения задач
| Задание | Рассчитайте молярную массу газа, плотность которого по воздуху равна 3,451. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2. Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. Dair(gas) = M(gas) / M(air); M(gas) = M(air) ×Dair(gas); M(gas) = 29 ×3,451 = 100,079 г/моль. |
| Ответ | Молярная масса газа равна 100,079 г/моль. |
| Задание | Определите молярную массу неизвестного газа, если равные объемы этого газа и хлора при одинаковых условиях имеют массы 4,87 г и 1,53 г. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2 или D = m1 / m2. Молярная масса водорода равна: Mr(Cl2) = 2 ×Ar(Cl) = 2 × 35,5 = 71. Тогда, молярная масса неизвестного газа DCl2 (gas) = m(gas) / m (Cl2) = 4,87 / 1,53 = 3,18. M (gas) = M(Cl2) ×DCl2 (gas) = 71×3,18 = 225,78 г/моль. |
| Ответ | Молярная масса газа равна 225,78 г/моль. |











