Плотность резины
Плотность резины и другие её физические свойства
Каучуки – полимеры сопряженных диеновых соединений. Промышленность производит много видов синтетических каучуков. Каучуки служат примером эластичных полимеров, обладающих способностью в широком температурном интервале подвергаться значительным обратимым деформациям.
Процесс вулканизации каучуков относится к так называемым реакциям сшивания, использующимся для образования мостиковых связей между линейными полимерными цепями, что приводит к образованию трехмерных сетчатых структур полимеров. Во время вулканизации для сшивки цепей полиизопрена в сырой каучук включается сера (3 – 8%), в результате чего образуются связи углерод-сера, причем сера может реагировать с двойными связями и реакционноспособными аллильными фрагментами полимерных цепей (рис. 1).
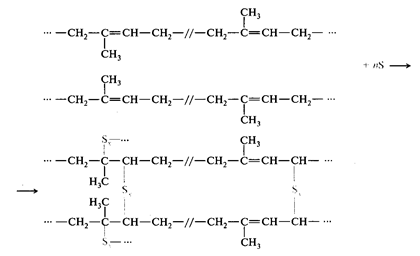
Рис. 1. Схема стадии вулканизации каучука для получения резины.
В зависимости от степени вулканизации различают мягкие (1 – 3% серы), полутвердые и твердые (более 30% серы) резины. Основные константы резины приведены ниже:
|
Плотность, кг/м3 |
900 – 1200 |
|
Модуль упругости, МПа |
1 – 10 |
|
Коэффициент Пуассона |
0,4 – 0,5 |
Резина применяется для изготовления шин для различных типов транспорта, уплотнителей шлангов, транспортерных лент, медицинских, и гигиенических изделий (рис. 2) и т.д.

Рис. 2. Изделие из резины.
Примеры решения задач
| Задание | Вычислите плотность озона O3 по азоту и по воздуху. |
| Решение | Для того, чтобы вычислить относительную плотность одного газа по другому, надо относительную молекулярную массу первого газа разделить на относительную молекулярную массу второго газа.
DN2(O3) = Mr(O3) / Mr(N2); DN2(O3) = 48 / 28 = 1,71. Dair(O3) = Mr(O3) / Mr(air); Dair(O3) = 48 / 29 = 1,66. Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. |
| Ответ | Плотность озона по азоту и по воздуху равна 1,66 и 1,71 соответственно. |
| Задание | Вычислите плотность а) по кислороду; б) по азоту; в) по воздуху следующих газов: аммиака NH3 и сернистого газа SO2. |
| Решение | Для того, чтобы вычислить относительную плотность одного газа по другому, надо относительную молекулярную массу первого газа разделить на относительную молекулярную массу второго газа.
Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. Mr(NH3) = Ar(N) + 3 ×Ar(H) = 14 + 3 ×1 = 14 + 3 = 17. Dair(NH3) = Mr(NH3) / Mr(air) = 17 / 29 = 0,59; DO2(NH3) = Mr(NH3) / Mr(O2) = 17 / 32 = 0,53; DN2(NH3) = Mr(NH3) / Mr(N2) = 17 / 28 = 0,61. Mr(O2) = 2 ×Ar(O) = 2 × 16 = 32. Mr(N2) = 2 ×Ar(N) = 2 × 14 = 28. 2) Mr(SO2) = Ar(S) + 2 ×Ar(O) = 32 + 2 ×16 = 32 + 32 = 64. Dair(SO2) = Mr(SO2) / Mr(air) = 64 / 29 = 2,21; DO2(SO2) = Mr(SO2) / Mr(O2) = 64 / 32 = 2; DH2(SO2) = Mr(SO2) / Mr(N2) = 64 / 28 = 2,29. |
| Ответ | Плотности аммиака по воздуху, кислороду и азоту соответственно равны 0,59, 0,53 и 0,61; плотности оксида серы (IV) по воздуху, кислороду и азоту соответственно равны 2,21, 2 и 2,29. |











