Плотность пропана
Плотность пропана и другие его физические свойства
С воздухом пропан образует взрывоопасные смеси, в случае если концентрация его паров находится в пределах 1,7 – 10,9%. При температуре 466oС и давлении 0,1 МПа (760 мм. рт. ст.) пропан самовоспламеняется на воздухе. Он легко сжижается и в виде смеси с другими газообразными алканами, например с бутаном, используется в быту как топливо (баллонный газ). Кроме этого, пропан применяется как автомобильное топливо.
Основные константы пропана приведены в таблице ниже.
Таблица 1. Физические свойства и плотность пропана.
|
Плотность, к/м3 |
1,8641(газ) 0,5005 (жидкость) [t = 20oC, Р = 4 атм] |
|
Температура плавления, oС |
-187,6 |
|
Температура кипения, oС |
-42,09 |
|
Молярная масса, г/моль |
44,1 |
Химический состав, строение молекулы и плотность пропана
Химический состав молекулы пропана можно отобразить эмпирической (C3H8) и рациональной (CH3-CH2-CH3) формулами (рис. 1).
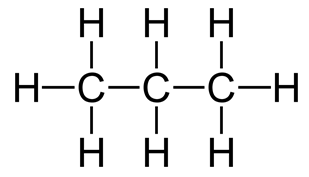
Рис. 1. Строение молекулы пропана.
В молекуле пропана гибридизации подвергаются одна s-орбиталь и три p-орбитали от каждого атома углерода. Вид и число орбиталей, участвующих в гибридизации определяет её тип. В пространстве эти орбитали расположены относительно друг друга под одинаковыми углами и направлены к вершинам тетраэдра.Тип гибридизации атомов углерода в молекуле пропана, как и в других алканах – sp3.
Примеры решения задач
| Задание | Плотность паров простого вещества азота по водороду – 14. Определите формулу азота. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2. Молярная масса газа равна его плотности по отношению к другому газу, умноженной на молярную массу второго газа: M1 = D×M2. Тогда, молярная масса газа азота будет равна: Mgas = DH2×M(H2) = 14× 2 = 28 г/моль. Mr(H2) = 2 ×Ar(H) = 2 × 1 = 2. Относительная атомная масса азота равна 14,0067 а.е.м. Тогда, в состав молекулы азота входит Mgas /Ar(P) атомов азота: Mgas / Ar(P) = 28 / 14,0067 = 2. Значит формула молекулы азота N2. |
| Ответ | Молярная масса азота равна 28 г/моль, а формула молекулы азота N2. |
| Задание | Плотность газа по воздуху – 0,59. Массовая доля элемента азота в нем – 82,35%, а водорода – 17,65%. Выведите формулу газа. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов азота в молекуле через «х», число атомов водорода через «у». Найдем соответствующие относительные атомные массы элементов азота и водорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(N) = 14; Ar(H) = 1. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y = ω(N)/Ar(N) : ω (H)/Ar(H); x:y = 82,35/14 : 17,65/1; x:y = 5,88 : 17,65 = 1 : 3. Значит простейшая формула соединения азота и водорода имеет вид NH3. Значение молярной массы газа можно определить при помощи его плотности по воздуху: Mgas = M(air) × Dair(gas); Mgas = 29 × 0,59 = 17,11 г/моль. Чтобы найти истинную формулу соединения азота и водорода найдем отношение полученных молярных масс: Mgas / M(NH3) = 17,11 / 17 = 1. M(NH3) = Ar(N) + 3 × Ar(H) = 14 + 3 × 1 = 14 + 3 = 17 г/моль. Таким образом формула вещества будет иметь вид NH3. Это аммиак. |
| Ответ | Формула газа — NH3. Это аммиак. |











