Плотность аммиака
Плотность аммиака и другие его физические свойства
Молекула аммиака имеет химический состав, который отражается формулой NH3. Он имеет форму тригональной пирамиды (dNH = 0,10нм, угол HNH = 107,30) (рис. 1). Согласно теории валентных связей это отвечает sp3-гибридизации валентных орбиталей атома азота. Из четырех sp3-гибридных орбиталей азота три участвуют в образовании трех σ-связей N-H, а четвертую орбиталь занимает не связывающая электронная пара. В терминах теории молекулярных орбиталей это соответствует заполнению трех связывающих и одной почти не связывающей молекулярной σ-орбитали:
σs2σx2σy2σz*2.
Поскольку не связывающее двухэлектронное облако ориентировано в пространстве, молекула аммиака – резко выраженный донор электронной пары и обладает высокой полярностью (m = 0,49×10-29 Кл×м).
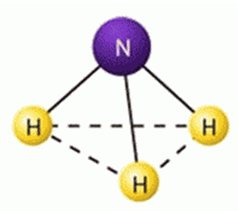
Рис. 1. Строение молекулы аммиака.
Полярность связи N-H обусловливает между молекулами аммиака водородную связь. Поэтому температуры плавления (-77,8oС) и кипения (-33,4oС) аммиака довольно высоки; он характеризуется значительной энтальпией испарения и легко сжижается.
Жидкий аммиак, как и вода, — сильно ионизирующий растворитель. При этом производные NH4+ в жидком аммиаке ведут себя как кислоты (аминокислоты), а производные NH2— — как основания (аммонооснования). Например, сильными кислотами в жидком аммиаке являются NH4Cl, NH4NO3, а основаниями – KNH2, Ba(NH2)2. Дигидронитриды Zn(NH2)2, Al(NH2)3ведут себя как амфотерные соединения.
Аммиак очень хорошо растворяется в воде (при 20oС в одном объеме воды растворяется около 700 объемов аммиака). Хорошая растворимость объясняется образованием водородной связи между молекулами NH3 и H2O.
Краткое описание химических свойств и плотность аммиака
Аммиак весьма реакционноспособен, склонен к реакциям присоединения.Сгорает в кислороде, реагирует с кислотами, металлами, галогенами, оксидами и галогенидами.
4NH3 + 3O2 = 2N2 + 6H2O (сгорание);
NH3 + HClg = NH4Clg;
NH3 + H2SO4 = NH4HSO4;
2NH3 + H2SO4 = (NH4)2SO4;
2NH3 + Cl2 = NH2Cl + NH4Cl (в атмосфере азота);
8NH3 + 3Cl2 = N2 + 6NH4Cl (сгорание);
2NH3 + CO2= NH4(NH2COO);
2NH3 + CO2 = C(NH2)2O + H2O (t = 180 – 500oC, p);
2NH3 + 2Na = 2NaNH2 + H2 (t = 350oC);
2NH3 + 2Mg = Mg3N2 + 3H2(t = 600 – 850oC);
2NH3 + 2Al = 2AlN + 3H2 (выше t = 600oC).
Качественная реакция на аммиак — почернение бумажки, смоченнойраствором Hg2(NO3)2 (образование ртути). Осушают аммиак оксидом кальция.
4NH3 (g) + H2O + 2Hg2(NO3)2 = (Hg2N)NO3×H2O↓ + 1Hg↓ + 3NH4NO3.
Жидкий аммиак — основный протонный растворитель; хорошо растворяетсеру, галогениды (кроме фторидов) и нитраты щелочных металлов, галогенидыаммония, перманганат калия; плохо растворяет неорганические фториды, сульфаты, карбонаты.
Примеры решения задач
| Задание | Рассчитайте молярную массу газа, плотность которого по воздуху равна 0,756. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2. Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. Dair(gas) = M(gas) / M(air); M(gas) = M(air) ×Dair(gas); M(gas) = 29 ×0,756 = 22 г/моль. |
| Ответ | Молярная масса газа равна 22 г/моль. |
| Задание | Определите молярную массу неизвестного газа, если равные объемы этого газа и кислорода при одинаковых условиях имеют массы 4,15 г и 0,32 г. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2 или D = m1 / m2. Молярная масса водорода равна: Mr(O2) = 2 ×Ar(O) = 2 × 16 = 32. Тогда, молярная масса неизвестного газа DO2 (gas) = m(gas) / m (O2) = 4,15 / 0,32 = 1,328. M (gas) = M(O2) ×DO2 (gas) = 32 ×1,328 = 42,5 г/моль. |
| Ответ | Молярная масса газа равна 42,5 г/моль. |











