Плотность ацетона
Плотность ацетона и другие его физические свойства
Кроме воды, ацетон хорошо растворяется в бензоле, метаноле, этаноле, диэтиловом эфире и многих сложных эфирах. Диметилкетон является хорошим растворителем для многих органических веществ, в частности нитроцеллюлозы и алкалоидов.
Основные константы ацетона приведены в таблице ниже.
Таблица 1. Физические свойства и плотность ацетона.
|
Плотность, г/см3 (20oС) |
0,7899 |
|
Температура плавления, oС |
-95 |
|
Температура кипения, oС |
56,1 |
|
Температура вспышки, oС |
-20 |
|
Температура самовоспламенения, oС |
465 |
|
Молярная масса, г/моль |
58,08 |
Ацетон находит широкое применение в качестве растворителя, используется как исходное вещество для синтеза хлороформа и иодоформа. Появляется в моче больных сахарным диабетом. Для его обнаружения используется иодоформная проба.
Химический состав и строение молекулы ацетона
Химический состав молекулы ацетона можно выразить при помощи эмпирической (C3H6O) и рациональной (CH3-C(O)-CH3) формул (рис. 1).
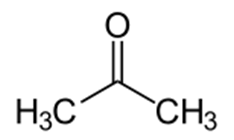
Рис. 1. Строение молекулы ацетона.
Как представитель класса кетонов ацетон относится к группе карбонильных соединений, т.е. имеющих в своем составе карбонильную группу (=C=O), которая соединена с двух сторон метильными радикалами.
Атомы углерода и кислорода карбонильной группы находятся в состоянии sp2 –гибридизации и связаны σ- и π-связями, составляющими двойную связь. π-Связь образуется в результате перекрывания негибридных p-орбиталей обоих атомов. Из шести валентных атомов кислорода один расходуется на образование σ-связи, второй – на образование π-связи. Две неподеленные пары электронов располагаются на гибридных орбиталях, которые лежат в плоскости σ-связей. Карбонильная группа и непосредственно связанные с ней атомы находятся в одной плоскости.
Краткое описание химических свойств и плотность ацетона
Ацетон – первый представитель гомологического ряда кетонов. Для него характерны реакции нуклеофильного присоединения-отщепления. Например, при присоединении гидроксиламина образуется оксим, гидразина – гидразон, а фенилгидразина – фенилгидразон:
CH3-C(O)-CH3 + NH2OH = (CH3)2-C=N-OH + H2O;
CH3-C(O)-CH3 + NH2NH2 = (CH3)2-C=N-NH2 + H2O;
CH3-C(O)-CH3 + NH2NHC6H5 = (CH3)2-C=N-NH-C6H5 + H2O;
Ацетон восстанавливается водородом в присутствии платины в качестве катализатора. Продуктом реакции является вторичный одноатомный спирт:
CH3-C(O)-CH3 = (H2/Pt) = CH3-CH(OH)-CH3.
Примеры решения задач
| Задание | Рассчитайте плотность оксида азота (IV) по водороду. |
| Решение | Для того, чтобы вычислить относительную плотность одного газа по другому, надо относительную молекулярную массу первого газа разделить на относительную молекулярную массу второго газа.
DH2(NO2) = Mr(NO2) / Mr(H2); DH2(NO2) = 46 / 2 = 23. Mr(NO2) = Ar(N) + 2 ×Ar(O) = 14 + 2 × 16 = 14 + 32 = 46. Mr(H2) = 2 ×Ar(H) = 2 × 1 = 2. |
| Ответ | Плотность оксида азота (IV) по водороду равна 23. |
| Задание | Определите во сколько раз тяжелее воздуха угарный газ CO. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа.
D = M1 / M2. Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов. Dair(CO) = Mr(CO) / Mr(air); Dair(CO) = 28 / 29 = 1,17. Mr(CO) = Ar(C) + Ar(O) = 12 + 16 = 0,96. |
| Ответ | Угарный газ CO легче воздуха в 0,96 раз. |











