Таблица молярных масс веществ
Таблица молярных масс веществ
![]()
Молярную массу обычно выражают в г/моль, реже в кг/кмоль. Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr):
M = κ × Mr,
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Относительная молекулярная масса – величина безразмерная. Её вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы:
Mr(HX) = Ar(H) + Ar(X).
M (HX) = Mr(HX) = Ar(H) + Ar(X).
Для того, чтобы легче не затрачивать каждый раз время на расчет молярной массы конкретного вещества используют таблицу молярных масс, которая выглядит следующим образом:
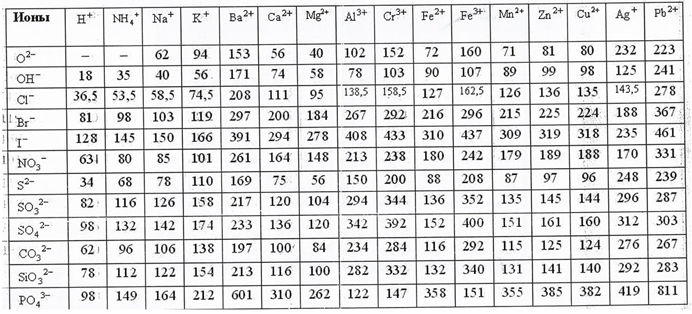
Примеры решения задач
| Задание | Составьте формулы двух оксидов меди, если массовые доли меди в них 79,9% и 88,8%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Найдем массовую долю в каждом из оксидов меди: ω1 (О) = 100% — ω1 (Cu) = 100% — 79,9% = 20,1%; ω2 (О) = 100% — ω2 (Cu) = 100% — 88,8% = 11,2%. Обозначим количество моль элементов, входящих в состав соединения за «х» (медь) и «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел): x:y = ω1 (Cu)/Ar(Cu) : ω1 (O)/Ar(O); x:y = 79,9/64 : 20,1/16; x:y = 1,25 : 1,25 = 1 : 1. Значит формула первого оксида меди будет иметь вид CuO. x:y = ω2 (Cu)/Ar(Cu) : ω2 (O)/Ar(O); x:y = 88,8/64 : 11,2/16; x:y = 1,39 : 0,7 = 2 : 1. Значит формула второго оксида меди будет иметь вид Cu2O. |
| Ответ | CuO и Cu2O |
| Задание | Составьте формулы двух оксидов железа, если массовые доли железа в них 77,8% и 70,0%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Найдем массовую долю в каждом из оксидов меди: ω1 (О) = 100% — ω1 (Fe) = 100% — 77,8% = 22,2%; ω2 (О) = 100% — ω2 (Fe) = 100% — 70,0% = 30,0%. Обозначим количество моль элементов, входящих в состав соединения за «х» (железо) и «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел): x:y = ω1 (Fe)/Ar(Fe) : ω1 (O)/Ar(O); x:y = 77,8/56 : 22,2/16; x:y = 1,39 : 1,39 = 1 : 1. Значит формула первого оксида железа будет иметь вид FeO. x:y = ω2 (Fe)/Ar(Fe) : ω2 (O)/Ar(O); x:y = 70/56 : 30/16; x:y = 1,25 : 1,875 = 1 : 1,5 = 2 : 3. Значит формула второго оксида железа будет иметь вид Fe2O3. |
| Ответ | FeO, Fe2O3 |











