Молярная масса воды
Молярная масса воды
Вода – это наиболее распространенное вещество в природе. Она представляет собой термодинамически устойчивое соединение, способное находиться сразу в трех агрегатных состояниях: жидком, твердом (лед) и газообразном (водяной пар), каждое из которых определяется температурой и давлением (рис. 1).
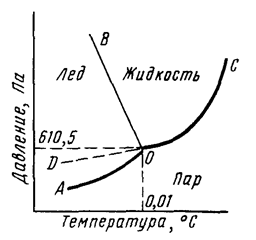
Рис. 1. Диаграмма состояния воды.
Кривая АО соответствует равновесию в системе лед-пар, DO – равновесию в системе переохлажденная вода-пар, кривая OC – равновесию в системе вода-пар, а кривая OB – равновесию в системе лед-вода. В точке О все кривые пересекаются. Эта точка называется тройной точкой и отвечает равновесию в системе лед-вода-пар.
Брутто-формула воды – H2O. Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Mr(H2O) = 2×Ar(H) + Ar(O);
Mr(H2O) = 2×1 + 16 = 2 + 16 = 18.
Легко показать, что численные значения молярной массы М и относительной молекулярной массы Mr равны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что молярная масса воды равна 18 г/моль.
Примеры решения задач
| Задание | Рассчитайте массовую долю элементов в следующих молекулах: а) воды (H2O); б) серной кислоты (H2SO4). |
| Ответ | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Рассчитаем массовые доли каждого из элементов, входящих в состав указанных соединений. а) Найдем молекулярную массу воды: Mr (H2O) = 2×Ar(H) + Ar(O); Mr (H2O) = 2×1,00794 + 15,9994 = 2,01588 + 15,9994 = 18,0159. Известно, что M = Mr, значит M(H2O) = 32,2529 г/моль. Тогда массовые доли кислорода и водорода будут равны: ω (H) = 2 × Ar (H) / M (H2O) × 100%; ω (H) = 2 × 1,00794 / 18,0159 × 100%; ω (H) = 2,01588 / 18,0159× 100% = 11,19%. ω (O) = Ar (O) / M (H2O) × 100%; ω (O) = 15,9994 / 18,0159× 100% = 88,81%. б) Найдем молекулярную серной кислоты: Mr (H2SO4) = 2×Ar(H) + Ar(S) + 4×Ar(O); Mr (H2SO4) = 2×1,00794 + 32,066 + 4×15,9994 = 2,01588 + + 32,066 + 63,9976; Mr (H2SO4) = 98,079. Известно, что M = Mr, значит M(H2SO4) = 98,079 г/моль. Тогда массовые доли кислорода, серы и водорода будут равны: ω (H) = 2 × Ar (H) / M (H2SO4) × 100%; ω (H) = 2 × 1,00794 / 98,079 × 100%; ω (H) = 2,01588 / 98,079× 100% = 2,06%. ω (S) = Ar (S) / M (H2SO4) × 100%; ω (S) = 32,066 / 98,079× 100% = 32,69%. ω (O) = 4×Ar (O) / M (H2SO4) × 100%; ω (O) = 4×15,9994 / 98,079× 100% = 63,9976/ 98,079× 100% = 65,25% |
| Задание | Вычислите, где каком из соединений массовая доля (в %) элемента водорода больше: в метане (CH4) или сероводороде (H2S)? |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Рассчитаем массовую долю каждого элемента водорода в каждом из предложенных соединений (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел). Найдем молекулярную массу метана: Mr (CH4) = 4×Ar(H) + Ar(C); Mr (CH4) = 4×1+ 12 = 4 + 12 = 16. Известно, что M = Mr, значит M(CH4) = 16 г/моль. Тогда массовая доля водорода в метане будет равна: ω (H) = 4 × Ar (H) / M (CH4) × 100%; ω (H) = 4 × 1 / 16 × 100%; ω (H) = 4/ 16 × 100% = 25%. Найдем молекулярную массу сероводорода: Mr (H2S) = 2×Ar(H) + Ar(S); Mr (H2S) = 2×1+ 32 = 2 + 32 = 34. Известно, что M = Mr, значит M(H2S) = 34 г/моль. Тогда массовая доля водорода в сероводороде будет равна: ω (H) = 2 × Ar (H) / M (H2S) × 100%; ω (H) = 2 × 1 / 34 × 100%; ω (H) =2/ 34 × 100% = 5,88%. Таким образом, массовая доля водорода больше в метане, поскольку 25 > 5,88. |
| Ответ | Массовая доля водорода больше в метане (25%) |











