Молярная масса криптона
Молярная масса криптона
Порядковый номер – 36. Строение атома показано на рис. 1. Относится к семейству инертных (благородных) газов.
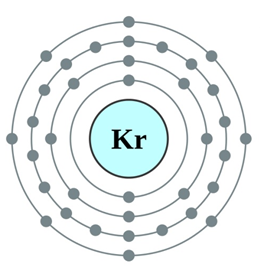
Рис. 1. Схема строения атома криптона.
Молярная масса криптона равна 83,798 г/моль, т.е именно столько «весит» один моль аргона. Данную величину также можно выразить в кг/кмоль.
Для того, чтобы вычислить молярную массу криптона можно использовать три способа:
1) Молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr), которую вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
M = κ × Mr,
где κ – коэффициент пропорциональности, одинаковый для всех веществ.
Т.е. определение молярной массы криптона сводится к нахождению его относительной атомной массы.
2) Криптон– газообразное вещество. Молекулярную массу газов можно определить при помощи величины молярного объема: необходимо найти объем, который занимает при нормальных условиях определенная масса криптона, а после вычислить массу 22,4 л криптона при тех же условиях.
3) Величину молярной массы криптона можно рассчитать при помощи уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
pV = mRT / M,
где p – давление газа (Па), V – объем газа (м3), m – масса вещества (г), M – молярная масса вещества (г/моль), Т – абсолютная температура (К), R – универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
| Задание | Рассчитайте относительную плотность по воздуху криптона. |
| Решение | Известно, что плотность какого-либо газа по воздуху рассчитывается как отношение молярной масса этого газа к молярной массе воздуха (29 г/моль):
Dair = M / Mair. Молярная масса криптона равна 84 г/моль. Тогда его плотность по воздуху будет равна: Dair (Kr) = M (Kr) / Mair; Dair (Kr) = 84 / 29 = 2,8966. |
| Ответ | Плотность криптона по воздуху равна 2,8966. |
| Задание | Вычислите энергию ионизации для иона криптона Kr(1s22s22p63s23p63d104s24p3). |
| Решение | Рассчитаем энергию ионизации иона аргона Kr(1s22s22p63s23p63d104s24p3):
ЕИ = R × z2 / n2, где R – константа Ридберга равная 13,6 эВ; z–заряд атома, n – число электронов в атоме. Порядковый номер криптона равен 36-ти, значит заряд атома криптона (+36). Количество электронов в данном ионе равно 33-м. ЕИ (Kr) = 13,6 × 362 / 332; ЕИ (Kr) = 13,6 × 1296 / 1089 = 16,19 эВ. |
| Ответ | 16,19 эВ |











