Молярная масса фосфора
Молярная масса фосфора
Порядковый номер – 15. Строение атома показано на рис. 1. Неметалл p-семейства.
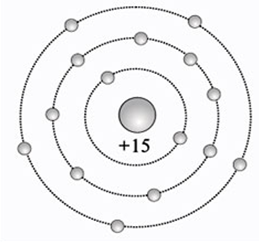
Рис. 1. Схема строения атома фосфора.
В обычных условиях фосфор может существовать в виде нескольких простых веществ – аллотропных модификаций: белого, красного и черного фосфора. Белый фосфор находится в твердом агрегатном состоянии, бесцветен и прозрачен. Легко окисляется на воздухе, вследствие чего светится в темноте. Ядовит. Красный фосфор медленно окисляется на воздухе, не светится в темноте и неядовит. Черный фосфор образуется из белого путем его нагревания под высоким давлением при 200-220oC. По внешнему виду похож на графит, жирный на ощупь.
Молярная масса фосфора равна 30,9738 г/моль. Эта величина показывает столько «весит» один моль данного элемента.
Молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr), которую вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
M = κ × Mr,
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Т.е. определение молярной массы фосфора сводится к нахождению его относительной атомной массы.
Примеры решения задач
| Задание | Вычислите массу фосфора, который надо сжечь в кислороде для получения оксида фосфора (V) массой 3,55 г? |
| Решение | Запишем уравнение реакции горения фосфора в кислороде с образованием оксида фосфора (V):
4P + 5O2 = 2P2O5. Рассчитаем количество вещества оксида фосфора (V) (молярная масса – 284 г/моль): n = m / M; n(P2O5) = m(P2O5) / M(P2O5); n(P2O5) = 3,55 / 284 = 0,0125 моль. Согласно уравнению реакции n(P2O5) : n(P) = 2:4, значит: n(P) = 2 × n(P2O5); n(P) = 2 × 0,0125 = 0,025 моль. Тогда, масса фосфора (молярная масса – 124 г/моль) будет равна: m = n × M; m(P) = n(P) × M(P); m(P) = 0,025 × 124 = 3,1г. |
| Ответ | Масса фосфора равна 3,1 г |
| Задание | Фосфин можно получить действием соляной кислоты на фосфид кальция. Рассчитайте объем фосфина (н.у.), который образуется из 9,1 г фосфида кальция. Массовая доля выхода продукта составляет 90%. |
| Решение | Запишем уравнение реакции получения фосфина из фосфида кальция:
Ca3P2 + 6HCl = 2PH3 + 3CaCl2. Рассчитаем количество вещества фосфида кальция (молярная масса – 182 г/моль): n = m / M; n(PH3) = m(PH3) / M(PH3); n(PH3) = 9,1 / 182 = 0,05 моль. Согласно уравнению реакции n(PH3) : n(Ca3P2) = 2:1, значит: n(PH3) = 2 × n(Ca3P2); n(PH3) = 2 × 0,05 = 0,1 моль. Тогда, объем выделившегося фосфина будет равен: V = n × Vm; V(PH3) = n (PH3) × Vm; V(PH3) = 0,1 × 22,4 = 2,24 л. Учитывая выход продукта реакции, объем фосфина составляет: V(PH3) = V(PH3) × η/100%; V(PH3) = 2,24 × 90/100% = 2,016 л. |
| Ответ | Объем фосфина равен 2,016 л |











