Молярная масса этанола
Молярная масса этанола
Строение молекулы показано на рис. 1. В обычных условиях представляет собой бесцветную летучую жидкость с характерным запахом и жгучим вкусом. Смешивается с водой и различными органическими растворителями, а также сам хорошо растворяет многие вещества (чаще органической природы).
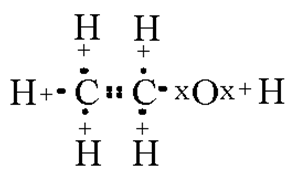
Рис. 1. Строение молекулы этанола.
Брутто-формула этанола – C2H5OH. Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Mr(C2H5OH) = 2×Ar(С) + 6×Ar(H) + Ar(O);
Mr(C2H5OH) = 2×12 + 6×1 + 16 = 24 + 6 + 16 = 46.
Молярная масса (М) – это масса 1 моль вещества. Легко показать, что численные значения молярной массы М и относительной молекулярной массы Mrравны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что молярная масса этанола равна 46 г/моль.
Примеры решения задач
| Задание | Составьте формулу соединения водорода, йода и кислорода, если массовые доли элементов в нём: ω(H) = 2,2%, ω(I) = 55,7%, ω(O) = 42,1%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (водород), «у» (йод), «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(H)/Ar(H) : ω(I)/Ar(I) : ω(O)/Ar(O); x:y:z= 2,2/1 : 55,7/127: 42,1/16; x:y:z= 2,2 : 0,44: 2,63 = 5 : 1 : 6. Значит формула соединения водорода, йода и кислорода будет иметь вид H5IO6. |
| Ответ | H5IO6 |
| Задание | Составьте формулу соединения натрия, фосфора и кислорода, если массовые доли элементов в нём: ω(Na) = 34,6%, ω(P) = 23,3%, ω(O) = 42,1%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (натрий), «у» (фосфор), «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(Na)/Ar(Na) : ω(P)/Ar(P) : ω(O)/Ar(O); x:y:z= 34,6/23 : 23,3/31: 42,1/16; x:y:z= 1,5 : 0,75: 2,63 = 2 : 1 : 3. Значит формула соединения натрия, фосфора и кислорода будет иметь вид Na2PO3. |
| Ответ | Na2PO3 |











