Молярная масса азотной кислоты
Молярная масса азотной кислоты
Строение молекулы азотной кислоты приведено на рис. 1. Смешивается с водой в любых соотношениях. Является сильным электролитом, т.е. в водном растворе практически полностью диссоциирует на ионы. В ОВР проявляет себя в роли окислителя.
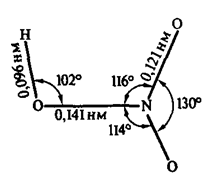
Рис. 1. Строение молекулы азотной кислоты с указанием валентных углов между связями и длин химических связей.
Брутто-формула азотной кислоты – HNO3. Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Mr(HNO3) = Ar(H) + Ar(N) + 3×Ar(O);
Mr(HNO3) = 1 + 14 + 3×16 = 1 + 14+ 48= 63.
Молярная масса (М) – это масса 1 моль вещества. Легко показать, что численные значения молярной массы М и относительной молекулярной массы Mr равны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что молярная масса азотной кислоты равна 63 г/моль.
Примеры решения задач
| Задание | Составьте формулу соединения магния, серы и кислорода, если соотношение масс элементов в нём m(Mg):m(S):m(O) = 3:4:8. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы магния, серы и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел). Известно, что M = Mr, значит (Mg) = 24 г/моль, M(S) = 32 г/моль, а М(O) = 16 г/моль. Тогда, количество вещества этих элементов равно: n (Mg) = m (Mg) / M (Mg); n (Mg) = 3 / 24 = 0,125 моль. n (S) = m (S) / M (S); n (S) = 4 / 32 = 0,125 моль. n (О) = m (О) / M (О); n (О) = 8 / 16 = 0,5 моль. Найдем мольное отношение: n(Mg) :n(S): n(О) = 0,125:0,125:0,5 = 1:1:4. т.е. формула соединения магния, серы и кислорода имеет вид MgSO4. Это сульфат магния. |
| Ответ | MgSO4 |
| Задание | Составьте формулу соединения серы с кислородом, если массовые доли элементов в нём: ω(S) = 40%, ω(O) = 60%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (сера) и «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел): x:y = ω(S)/Ar(S) : ω(O)/Ar(O); x:y = 40/32 : 60/16; x:y = 1,25 : 3,75 = 1 : 3. Значит формула соединения серы с кислородом будет иметь вид SO3. Это оксид серы (VI). |
| Ответ | SO3 |











