Общая характеристика химических элементов
Характеристика химических элементов в зависимости от строения их атомов
Все химические элементы можно охарактеризовать в зависимости от строения их атомов, а также по их положению в Периодической системе Д.И. Менделеева. Обычно характеристику химического элемента дают по следующему плану:
- указывают символ химического элемента, а также его название;
- исходя из положения элемента в Периодической системе Д.И. Менделеева указывают его порядковый, номер периода и группы (тип подгруппы), в которых находится элемент;
- исходя из строения атома указывают заряд ядра, массовое число, число электронов, протонов и нейтронов в атоме;
- записывают электронную конфигурацию и указывают валентные электроны;
- зарисовывают электронно-графические формулы для валентных электронов в основном и возбужденном (если оно возможно) состояниях;
- указывают семейство элемента, а также его тип (металл или неметалл);
- указывают формулы высших оксидов и гидроксидов с кратким описанием их свойств;
- указывают значения минимальной и максимальной степеней окисления химического элемента.
Характеристика химического элемента на примере ванадия (V)
Рассмотрим характеристику химического элемента на примере ванадия (V) согласно плану, описанному выше:
1. V – ванадий.
2. Порядковый номер – 23. Элемент находится в 4 периоде, в V группе, А (главной) подгруппе.
3. Z=23 (заряд ядра), M=51 (массовое число), e=23 (число электронов), p=23 (число протонов), n=51-23=28 (число нейтронов).
4.23V 1s22s22p63s23p63d34s2 – электронная конфигурация, валентные электроны 3d34s2.
5. Основное состояние
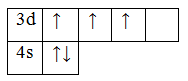
Возбужденное состояние
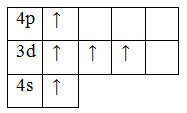
6. d-элемент, металл.
7. Высший оксид – V2O5 — проявляет амфотерные свойства, с преобладанием кислотных:
V2O5 + 2NaOH = 2NaVO3 + H2O
V2O5 + H2SO4 = (VO2)2SO4 + H2O (рН<3)
Ванадий образует гидроксиды следующего состава V(OH)2, V(OH)3, VO(OH)2. Для V(OH)2 и V(OH)3 характерны основные свойства (1, 2), а VO(OH)2 обладает амфотерными свойствами (3, 4):
V(OH)2 + H2SO4 = VSO4 + 2H2O (1)
2 V(OH)3 + 3 H2SO4 = V2(SO4)3 + 6 H2O (2)
VO(OH)2 + H2SO4 = VOSO4 + 2 H2O (3)
4 VO(OH)2 + 2KOH = K2[V4O9] + 5 H2O (4)
8. Минимальная степень окисления «+2», максимальная – «+5»
Примеры решения задач
| Задание | Охарактеризуйте химический элемент фосфор |
| Решение | 1. P – фосфор.
2. Порядковый номер – 15. Элемент находится в 3 периоде, в V группе, А (главной) подгруппе. 3. Z=15 (заряд ядра), M=31 (массовое число), e=15 (число электронов), p=15 (число протонов), n=31-15=16 (число нейтронов). 4.15P 1s22s22p63s23p3 – электронная конфигурация, валентные электроны 3s23p 3. 5. Основное состояние 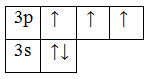
Возбужденное состояние 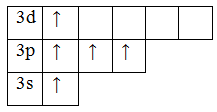
6. p-элемент, неметалл. 7. Высший оксид – P2O5 — проявляет кислотные свойства: P2O5 + 3Na2O = 2Na3PO4 Гидроксид, соответствующий высшему оксиду – H3PO4, проявляет кислотные свойства: H3PO4 + 3NaOH = Na3PO4 + 3H2O 8. Минимальная степень окисления «-3», максимальная – «+5» |
| Задание | Охарактеризуйте химический элемент калий |
| Решение | 1. K – калий.
2. Порядковый номер – 19. Элемент находится в 4 периоде, в I группе, А (главной) подгруппе. 3. Z=19 (заряд ядра), M=39 (массовое число), e=19 (число электронов), p=19 (число протонов), n=39-19=20 (число нейтронов). 4.19K 1s22s22p63s23p64s1 – электронная конфигурация, валентные электроны 4s 1. 5. Основное состояние 
6. s-элемент, металл. 7. Высший оксид – K2O — проявляет основные свойства: K2O + SO2 = K2SO4 K2O + 2HCl = 2KCl + H2O Гидроксид, соответствующий высшему оксиду – KOH, проявляет основные свойства: KOH + HNO3 = KNO3 + H2O 2KOH+ N2O5 = 2KNO3 + H2O 8. Cтепень окисления «+1» |











