Строение атома технеция
Общие сведения о строении атома технеция
Относится к элементам d-семейства. Металл. Обозначение – Tc. Порядковый номер – 43. Относительная атомная масса – 99 а.е.м.
Электронное строение атома технеция
Атом технеция состоит из положительно заряженного ядра (+43), внутри которого есть 43 протона и 56 нейтронов, а вокруг, по пяти орбитам движутся 43 электрона.
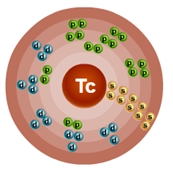
Рис.1. Схематическое строение атома технеция.
Распределение электронов по орбиталям выглядит следующим образом:
+43Tc)2)8)18)13)2;
1s22s22p63s23p63d104s24p64d55s2.
Внешний энергетический уровень атома технеция содержит 7 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
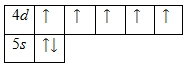
Валентные электроны атома технеция можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
5 |
0 |
0 |
+1/2 |
|
s |
5 |
0 |
0 |
-1/2 |
|
d |
4 |
2 |
-2 |
+1/2 |
|
d |
4 |
2 |
-1 |
+1/2 |
|
d |
4 |
2 |
0 |
+1/2 |
|
d |
4 |
2 |
+1 |
+1/2 |
|
d |
4 |
2 |
+2 |
+1/2 |
Примеры решения задач
| Задание | У какого элемента четвертого периода – хрома или селена – сильнее выражены металлические свойства? Запишите их электронные формулы. |
| Ответ | Запишем электронные конфигурации основного состояния хрома и селена:
24Cr 1s22s22p63s23p63d54s1; 34Se 1s22s22p63s23p63d104s24p4. Металлические свойства сильнее выражены у селена, чем у хрома. Правдивость данного утверждения можно доказать с помощью Периодического закона, согласно которому при переходе в группе сверху вниз металлические свойства элемента возрастают, а неметаллические убывают, что связано с тем, что при продвижении вниз по группе в атоме возрастает число электронных слоев, вследствие чего валентные электроны слабее удерживаются ядром. |
| Задание | Сколько атомных орбиталей f-подуровня заполнено у элемента с порядковым номером 69? Запишите его электронную формулу. |
| Решение | На f-подуровне имеется семь орбиталей, на каждой из которых может одновременно находиться 2 электрона (14 в сумме). Элемент с порядковым номером 69 – это Туллий (Tm). Запишем электронную формулу атома туллия в основном состоянии:
[Xe]4f136s1 (сокращенная); 1s22s22p63s23p63d104s24p64d104f135s25p66s1. В атоме туллия на каждой орбитали f-подуровня имеются электроны. |
| Ответ | На каждой орбитали f-подуровня имеются электроны. |











