Строение атома сурьмы
Общие сведения о строении атома сурьмы
Относится к элементам p-семейства. Полуметалл. Обозначение – Sb. Порядковый номер – 51. Относительная атомная масса – 121,75 а.е.м.
Электронное строение атома сурьмы
Атом сурьмы состоит из положительно заряженного ядра (+51), внутри которого есть 51 протон и 71 нейтрон, а вокруг, по пяти орбитам движется 51 электрон.
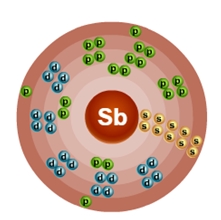
Рис.1. Схематическое строение атома сурьмы.
Распределение электронов по орбиталям выглядит следующим образом:
+51Sb)2)8)18)18)5;
1s22s22p63s23p63d104s24p64d105s25p3.
Внешний энергетический уровень атома сурьмы содержит 5 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
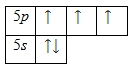
Наличие трех неспаренных электронов свидетельствует о том, что для сурьмы характерна степень окисления +3. За счет наличия вакантных орбиталей 5d-подуровня для атома сурьмы возможно возбужденное состояние (степень окисления +5):
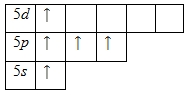
Валентные электроны атома сурьмы можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
5 |
0 |
0 |
+1/2 |
|
s |
5 |
0 |
0 |
-1/2 |
|
p |
5 |
1 |
-1 |
+1/2 |
|
p |
5 |
1 |
0 |
+1/2 |
|
p |
5 |
1 |
+1 |
+1/2 |
Примеры решения задач
| Задание | Медь имеет два изотопа: 63Cu (массовая доля равна 73%) и 65Сu (27%). Рассчитайте среднюю относительную атомную массу меди. |
| Решение | Изотопы – это атомы одного и того же химического элемента, имеющие разные массовые числа (одинаковое число протонов, но разное – нейтронов). Средняя относительная масса изотопов рассчитывается по формуле:
Ar = (Ar1 × ω1 + Ar2 × ω2)/100. Рассчитываем среднюю относительную атомную массу меди: Ar(Cu) = (63 × 73+ 65 × 27)/100; Ar(Cu) = (4725+ 1755)/100; Ar(Cu) = 6480/100 = 64,8 а.е.м. |
| Ответ | Ar(Cu) = 64,8 а.е.м. |
| Задание | Определите относительную атомную массу элемента кремния, если он состоит из трех изотопов: 28Si (молярная масса 92,3%), 29Si (4,7%) и 30Si (3,0%). |
| Решение | Изотопы – это атомы одного и того же химического элемента, имеющие разные массовые числа (одинаковое число протонов, но разное – нейтронов). Средняя относительная масса изотопов рассчитывается по формуле:
Ar = (Ar1 × ω1 + Ar2 × ω2 + Ar3 × ω3)/100. Рассчитываем среднюю относительную атомную массу кремния: Ar(Si) = (28 × 92,3+ 29 × 4,7 + 30 × 3,0)/100; Ar(Si) = (2584,4+ 136,3 + 90)/100; Ar(Si) = 2810,7/100 = 28,107 а.е.м. |
| Ответ | Ar(Si) = 28,107 а.е.м. |











