Пространственное строение алкенов
Общие сведения о пространственном строении алкенов
Эти соединения подчиняются общей формуле CnH2n, а в их названии присутствует суффикс –ен. Гомологический ряд алкенов начинается с этилена (этен) C2H6.
По сравнению с алканами, алкены характеризуются более низкими температурами плавления и кипения. Внутри гомологического ряда эти физические величины возрастают. Алкены, имеющие в своем составе от 2-х до 4-х атомов углерода представляют собой газы, от 5-ти до 17-ти – жидкости, более 17-ти – твердые вещества.
Пространственное строение
Атомы углерода при двойной связи в молекулах алкенов находятся в состоянии sp2-гибридизации. Двойная связь между ними образована из двух пар обобществленных электронов, т.е. это четырехэлектронная связь. Она сочетанием ковалентных σ-связи и π-связи. σ-Связь образована за счет осевого перекрывания sp2-гибридных орбиталей, а π-связь – за счет бокового перекрывания негибридизованныхp-орбителей двух атомов углерода (рис. 1).
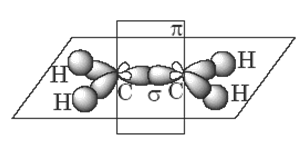
Рис. 1. Пространственное строение алкенов на примере молекулы этена.
Пять σ-связей двух sp2-гибридизованных атомов углерода лежат в одной плоскости под углом 120o и составляют σ-скелет молекулы. Над и под этой плоскостью симметрично расположена электронная плотность π-связи, которую можно изобразить также в виде плоскости, перпендикулярной σ-скелету.
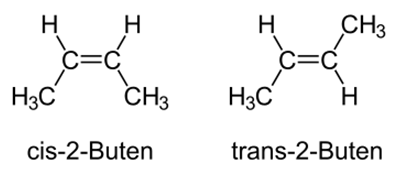
Для алкенов также характерно наличие пространственной изомерии, что обусловлено не только присутствием двойной связи, но и различным расположением заместителей относительно плоскости π-связи. Многие алкены могут существовать в виде цис- и транс-изомеров.
Цис- и транс-изомеры не являются структурными изомерами так как они имеют одинаковую последовательность связей атомов, а различаются расположением атомов или групп в пространстве, т.е. представляют собой пространственные изомеры (стереоизомеры). Например, цис-бутен-2, у которого два метильных заместителя расположены по одну и ту же сторону плоскости π-связи, и транс-бутен – 2, у которого эти заместителя располагаются по разные стороны плоскости π-связи:
Примеры решения задач
| Задание | Напишите уравнения реакций между пропиленом и следующими веществами: а) хлором; б) йодоводородом; в) этаном (в присутствии хлорида алюминия); г) водой. |
| Ответ | а) В результате взаимодействия пропилена с хлором происходит реакция присоединения в результате которой образуется 1,2-дихлорпропан:
H2C = CH – CH3 + Cl2 → ClH2C – CHCl– CH3. б)В результате взаимодействия пропилена сйодоводородом происходит образование 2-йодпропана: H2C = CH – CH3 +HI → H3C -CHI – CH3. в)В результате взаимодействия пропилена с этаном (в присутствии хлорида алюминия) происходит образование 2-метилпропана: H2C = CH – CH3 +С2H6 (AlCl3) → H3C -CH(CH3) – CH3. г) В результате взаимодействия пропилена с водой происходит образование пропан — 2-ола: H2C = CH – CH3 +H2O → H3C -CH(OH) – CH3. |
| Задание | Рассчитайте массу продукта, полученного при присоединении бромоводорода к 11,2 л пропилена (н.у.). Какой продукт образуется в этой реакции? | |
| Решение | Запишем уравнение реакции присоединения бромоводорода к пропилену, в результате которой образуется 2-бромпропан:
H2C = CH – CH3 +HBr → H3C -CHI – CH3. Рассчитаем количество вещества пропилена: n = V / Vm; n(C3H6) = V(C3H6) / Vm; n(C3H6) = 11,2 / 22,4 = 0,5моль. Согласно уравнению реакции n(C3H6) : n(C3H7Br) = 1:1, т.е. n(C3H6) = n(C3H7Br) = 0, 5 моль. Тогда масса 2-бромпропана будет равна (молярная масса – 123 г/моль): m = n × M; m(C3H7Br) = n(C3H7Br) × M; m(C3H7Br) = 0,5 × 123 = 61,5 г. |
|
| Ответ | Масса 2-бромпропана равна 61,5 г. |











