Строение атома платины
Общие сведения о строении атома платины
Относится к элементам d-семейства. Металл. Обозначение – Pt. Порядковый номер – 78. Относительная атомная масса – 195,84 а.е.м.
Электронное строение атома платины
Атом платины состоит из положительно заряженного ядра (+78), внутри которого есть 78 протонов и 118 нейтронов, а вокруг, по шести орбитам движутся 78 электронов.
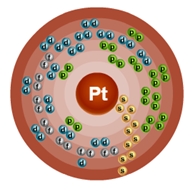
Рис.1. Схематическое строение атома платины.
Распределение электронов по орбиталям выглядит следующим образом:
+78Pt)2)8)18)32)17)1;
1s22s22p63s23p63d104s24p64f145s25p65d96s1.
Валентными электронами платины являются расположенные на 5d— и 6s-подуровнях электроны. Энергетическая диаграмма основного состояния принимает следующий вид:
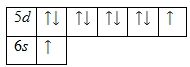
Валентные электроны атома платины можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
6 |
0 |
0 |
+1/2 |
|
d |
5 |
2 |
-2 |
+1/2 |
|
d |
5 |
2 |
-1 |
+1/2 |
|
d |
5 |
2 |
0 |
+1/2 |
|
d |
5 |
2 |
+1 |
+1/2 |
|
d |
5 |
2 |
+2 |
+1/2 |
|
d |
5 |
2 |
-2 |
-1/2 |
|
d |
5 |
2 |
-1 |
-1/2 |
|
d |
5 |
2 |
0 |
-1/2 |
|
d |
5 |
2 |
+1 |
-1/2 |
Примеры решения задач
| Задание | Природная платина состоит из шести стабильных изотопов: 190Pt (массовая доля равна 0,014%), 192Pt (0,782%), 194Pt(32,967%), 195Pt(33,832%), 196Pt(25,242%) и 198Pt (7,163%). Рассчитайте среднюю относительную атомную массу платины. |
| Решение | Изотопы – это атомы одного и того же химического элемента, имеющие разные массовые числа (одинаковое число протонов, но разное – нейтронов). Средняя относительная масса изотопов рассчитывается по формуле:
Ar = (Ar1 × ω1 + Ar2 × ω2+ Ar3 × ω3+ Ar4 × ω4+ Ar5 × ω5+ Ar6 × ω6)/100. Рассчитываем среднюю относительную атомную массу платины: Ar(Pt)= (190 × 0,014 + 192 × 0,782 + 194 × 32,967 + 195 × 33,832 + 196 × 25,242 + 198 × 7,163)/100; Ar (Pt)= (2,66 + 150,144 + 6395,598 + 6597,2985 + 4947,432 + 1418,274)/100; Ar (Pt)=195,114 а.е.м. |
| Ответ | Ar(Pt) = 195,114 а.е.м. |
| Задание | Назовите элементы, атомы которых имеют электронные конфигурации:
а) ls22s22p63s23p3; б) ls22s22p63s23p64s23d2; в) [Ar]3d54s2; г) [Х ]4f145d26s2. |
| Ответ | Чтобы определить порядковый номер химического элемента по его электронной конфигурации, записанной в форме а) и б), нужно сложить все электроны. Если же конфигурация записана, как в случае в) или г), надо прибавить к порядковому номеру элемента, указанного в квадратных скобках число электронов, «привязанных» к орбиталям.
а) всего 15 электронов, значит это фосфор; б) всего 22 электрона, значит это титан; в) всего 25 электронов, значит это марганец; г) всего 72 электрона, значит это гафний. |











