Строение атома ксенона
Общие сведения о строении атома ксенона
Относится к семейству инертных (благородных газов). Обозначение – Xe. Порядковый номер – 54. Относительная атомная масса – 131,3 а.е.м.
Электронное строение атома ксенона
Атом ксенона состоит из положительно заряженного ядра (+54), внутри которого есть 54 протона и 77 нейтронов, а вокруг, по пяти орбитам движется 54 электрона.
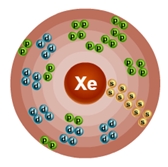
Рис.1. Схематическое строение атома ксенона.
Распределение электронов по орбиталям выглядит следующим образом:
+54Xe)2)8)18)18)8;
1s22s22p63s23p63d104s24p64d105s25p6.
Внешний энергетический уровень атома ксенона содержит 8 электронов, т.е. полностью завершен (именно поэтому ксенон мало химически активный элемент). Все эти электроны являются валентными. Возбужденного состояния нет. Энергетическая диаграмма основного состояния принимает следующий вид:
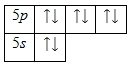
Валентные электроны атома ксенона можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
5 |
0 |
0 |
+1/2 |
|
s |
5 |
0 |
0 |
-1/2 |
|
p |
5 |
1 |
-1 |
+1/2 |
|
p |
5 |
1 |
0 |
+1/2 |
|
p |
5 |
1 |
+1 |
+1/2 |
|
p |
5 |
1 |
-1 |
-1/2 |
|
p |
5 |
1 |
0 |
-1/2 |
|
p |
5 |
1 |
+1 |
-1/2 |
Примеры решения задач
| Задание | Электронная формула аниона Э2- [10Ne]3s23p6 отвечает элементу: аргон, хлор, сера или фосфор? |
| Решение | Для того, чтобы записать полную электронную формулу искомого элемента, нужно знать электронную конфигурацию неона:
10Ne 1s22s22p6. Тогда, полная электронная формула имеет вид: 1s22s22p63s23p6. Так как при образовании отрицательно заряженных ионов элемент выступает в качестве акцептора протонов, то электронная формула элемента в основном состоянии имеет вид: 1s22s22p63s23p4. Общее количество электронов в электронной оболочке совпадает с порядковым номером элемента в Периодической таблице. Оно равно 16. Это сера. |
| Ответ | Сера (S) |
| Задание | Электронная формула аниона Э3+ 1s22s22p63s23p63d2 отвечает элементу: мышьяк, марганец, железо или ванадий? |
| Решение | Для элементов d-семейства валентными также являются электроны 4s-орбитали. Так как при образовании положительно заряженных ионов элемент выступает в качестве донора протонов, то электронная формула элемента в основном состоянии имеет вид:
1s22s22p63s23p63d34s2. Общее количество электронов в электронной оболочке совпадает с порядковым номером элемента в Периодической таблице. Оно равно 23. Это ванадий. |
| Ответ | Ванадий (V) |











