Строение атома калия
Общие сведения о строении атома калия
Относится к элементам s — семейства. Металл. Элементы-металлы, входящие в эту группу, носят общее название щелочных. Обозначение – K. Порядковый номер – 19. Относительная атомная масса – 39,102 а.е.м.
Электронное строение атома калия
Атом калия состоит из положительно заряженного ядра (+19), внутри которого есть 19 протонов и 20 нейтронов, а вокруг, по 4-м орбитам движутся 19 электронов.
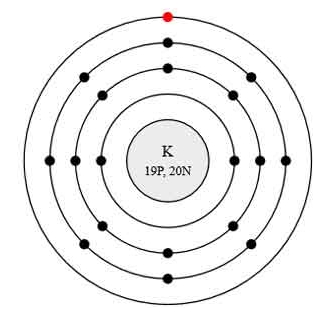
Рис.1. Схематическое строение атома калия.
Распределение электронов по орбиталям выглядит следующим образом:
1s22s22p63s23p64s1.
Внешний энергетический уровень атома калия содержит 1 электрон, который является валентным. Степень окисления калия равна +1. Энергетическая диаграмма основного состояния принимает следующий вид:

Возбужденного состояния, несмотря на наличие вакантных 3p— и 3d-орбиталей нет.
Примеры решения задач
| Задание | Атом элемента имеет следующую электронную конфигурацию 1s22s22p63s23p63d104s24p3. Укажите: а) заряд ядра; б) число завершенных энергетических уровней в электронной оболочке этого атома; в) максимально возможную степень окисления; г) валентность атома в соединении с водородом. |
| Решение | Для того, чтобы ответить на поставленные вопросы, сначала нужно определить общее число электронов в атоме химического элемента. Это можно сделать, сложив все электроны, имеющиеся в атоме, не учитывая их распределения по энергетическим уровням:
2+2+6+2+6+10+2+3 = 33. Это мышьяк (As). Теперь ответим на вопросы: а) заряд ядра равен +33; б) атом имеет четыре уровня, из которых завершенными являются три; в) запишем энергетическую диаграмму для валентных электронов атома мышьяка в основном состоянии. 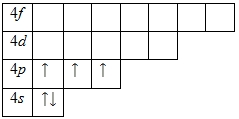
Мышьяк способен переходит в возбужденное состояние: электроны s-подуровня распариваются и один из них переходит на вакантную d-орбиталь. 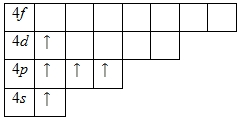
Пять неспаренных электронов свидетельствуют о том, что максимально возможная степень окисления мышьяка равна +5; г) Валентность мышьяка в соединении с водородом равна III (AsH3). |
| Задание | Напишите электронные формулы атомов: а) третьегоp-элемента четвертого периода; б) второго s-элемента пятого периода; в) девятого d-элемента четвертого периода. |
| Ответ | а) Третийp-элемент четвертого периода – это мышьяк 33As.
1s22s22p63s23p63d104s24p3 б) Второй s-элемент пятого периода – это стронций 38Sr. 1s22s22p63s23p63d104s24p65s2 в) Девятый d-элемент четвертого периода – это медь 29Cu. 1s22s22p63s23p63d104s1. |











