Строение атома кадмия
Общие сведения о строении атома кадмия
Относится к элементам d-семейства. Металл. Обозначение – Cd. Порядковый номер – 48. Относительная атомная масса – 112,41 а.е.м.
Электронное строение атома кадмия
Атом кадмия состоит из положительно заряженного ядра (+48), внутри которого есть 48 протонов и 64 нейтрона, а вокруг, по пяти орбитам движутся 48 электронов.
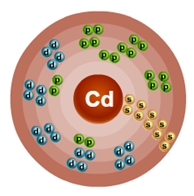
Рис.1. Схематическое строение атома кадмия.
Распределение электронов по орбиталям выглядит следующим образом:
+48Cd)2)8)18)18)2;
1s22s22p63s23p63d104s24p64d105s2.
Валентными электронами атома кадмия считаются электроны, расположенные на 4d— и 5s-орбиталях. Энергетическая диаграмма основного состояния принимает следующий вид:
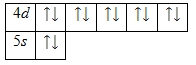
Валентные электроны атома кадмия можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
5 |
0 |
0 |
+1/2 |
|
s |
5 |
0 |
0 |
-1/2 |
|
d |
4 |
2 |
-2 |
+1/2 |
|
d |
4 |
2 |
-1 |
+1/2 |
|
d |
4 |
2 |
0 |
+1/2 |
|
d |
4 |
2 |
+1 |
+1/2 |
|
d |
4 |
2 |
+2 |
+1/2 |
|
d |
4 |
2 |
-2 |
-1/2 |
|
d |
4 |
2 |
-1 |
-1/2 |
|
d |
4 |
2 |
0 |
-1/2 |
|
d |
4 |
2 |
+1 |
-1/2 |
|
d |
4 |
2 |
+2 |
-1/2 |
Примеры решения задач
| Задание | Сколько атомных орбиталей p-подуровня заполнено у элементов с порядковыми номерами 35 и 54? Запишите их электронные формулы. |
| Ответ | Элементы с порядковыми номерами 35 и 54 – это бром и ксенон. Запишем их электронный формулы в основном состоянии:
35Br1s22s22p63s23p63d104s24p5; 54Xe1s22s22p63s23p63d104s24p64d105s25p6. На р-подуровне имеется 3 орбитали, на каждой из которых может располагаться не более 2-х электронов (6 в сумме). У атомов брома и ксенона p-орбитали заполнены. |
| Задание | Какие значения могут принимать квантовые числа n, l, ml иms, характеризующие состояние электронов в атоме. Какие значения они принимают для внешних электронов атома кальция? | |||||||||||||||
| Ответ | Главное квантовое число n может принимать значения от 1 и до бесконечности, но в реальности его пределом является число 7. Орбитальное квантовое число l может принимать значения от 0 до 3. Магнитное квантовое число mlпринимает значения от –l через 0 до +l. У спинового квантового числа ms может быть всего два значения: +1/2 и -1/2.
Запишем электронную конфигурацию основного состояния атома магния (валентные электроны выделим жирным шрифтом): 1s22s22p63s23p64s2. Электроны внешнего энергетического уровня будут характеризоваться следующим набором квантовых чисел:
|











