Строение атома индия
Общие сведения о строении атома индия
Относится к элементам p-семейства. Металл. Обозначение – In. Порядковый номер – 49. Относительная атомная масса – 114,82 а.е.м.
Электронное строение атома индия
Атом индия состоит из положительно заряженного ядра (+49), внутри которого есть 49 протонов и 66 нейтронов, а вокруг, по пяти орбитам движутся 49 электронов.
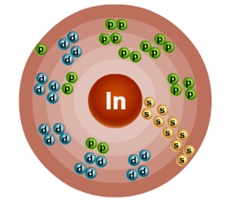
Рис.1. Схематическое строение атома индия.
Распределение электронов по орбиталям выглядит следующим образом:
+49In)2)8)18)18)3;
1s22s22p63s23p63d104s24p64d105s25p1.
Внешний энергетический уровень атома индия содержит 3 электрона, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
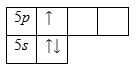
Валентные электроны атома индия можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
5 |
0 |
0 |
+1/2 |
|
s |
5 |
0 |
0 |
-1/2 |
|
p |
5 |
1 |
-1 |
+1/2 |
Примеры решения задач
| Задание | Электронная формула атома германия в основном состоянии имеет вид:
1)1s22s22p63s23p63d64s24p6; 2)1s22s22p63s23p63d64s24p2; 3)1s22s22p63s23p63d104s24p2; 4)1s22s22p63s23p63d104p4. |
| Ответ | Порядковый номер германия в Периодической таблице равен 32. Этот элемент относится к p-семейству, следовательно, сокращенная электронная формула должна иметь вид nsxnpy. Т.е., вариант под номер 4 не верный.
Германий находится в 4-м периоде и четвертой группе. Значит значение наибольшего главного квантового числа равно 4-м, а на внешнем энергетическом уровне имеется 4 электрона. Таким образом, верным является ответ 2: 1s22s22p63s23p63d64s24p2. |
| Задание | Напишите электронные формулы атомов серы, иттрия, ванадия и церия. Укажите семейство, к которому относится элемент, объясните его положение в Периодической системе, приведите электронно-графические формулы для валентных электронов. |
| Ответ | Сера.
1s22s22p63s23p4. Валентные электроны выделены жирным шрифтом. Относится к семейству р-элементов. Так как наибольшее главное квантовое число равно 3-м, а число электронов на внешнем энергетическом уровне равно 6-ти, сера расположена в 3-м периоде, VIA группе Периодической таблицы. Энергетическая диаграмма для валентных электронов имеет вид: 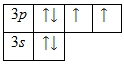
Иттрий. 1s22s22p63s23p63d104s24p64d15s2. Валентные электроны выделены жирным шрифтом. Относится к семейству d-элементов. Так как наибольшее главное квантовое число равно 5-ти, а число электронов на внешнем энергетическом уровне равно 3-м, иттрий расположен в 5-м периоде, IIIB группе Периодической таблицы. Энергетическая диаграмма для валентных электронов имеет вид: 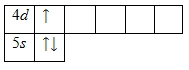
Ванадий. 1s22s22p63s23p63d34s2. Валентные электроны выделены жирным шрифтом. Относится к семейству d-элементов. Так как наибольшее главное квантовое число равно 4-м, а число электронов на внешнем энергетическом уровне равно 5-ти, ванадий расположен в 4-м периоде, VВ группе Периодической таблицы. Энергетическая диаграмма для валентных электронов имеет вид: 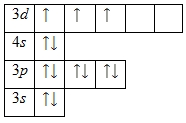
|











