Строение атома брома
Общие сведения о строении атома брома
Относится к элементам p-семейства. Неметалл. Обозначение – Br. Порядковый номер – 35. Относительная атомная масса – 79,904 а.е.м.
Электронное строение атома брома
Атом брома состоит из положительно заряженного ядра (+35), внутри которого есть 35 протонов и 45 нейтронов, а вокруг, по четырем орбитам движутся 35 электронов.
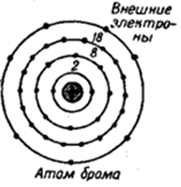
Рис.1. Схематическое строение атома брома.
Распределение электронов по орбиталям выглядит следующим образом:
+35Br)2)8)18)7;
1s22s22p63s23p63d104s24p5.
Внешний энергетический уровень атома брома содержит 7 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
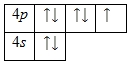
Каждый валентный электрон атома брома можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
4 |
0 |
0 |
+1/2 |
|
s |
4 |
0 |
0 |
-1/2 |
|
p |
4 |
1 |
-1 |
+1/2 |
|
p |
4 |
1 |
-1 |
-1/2 |
|
p |
4 |
1 |
0 |
+1/2 |
|
p |
4 |
1 |
0 |
-1/2 |
|
p |
4 |
1 |
1 |
+1/2 |
Наличие одного неспаренного электрона свидетельствует о том, что степень окисления брома может быть равна -1 или +1. Так как на четвертом уровне есть вакантные орбитали 4d-подуровня, то для атома брома характерно наличие возбужденного состояния:
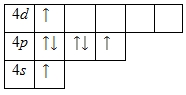
Именно поэтому для брома также характерна степень окисления +3. Известно, что в своих соединениях бром также способен проявлять степени окисления +5 и +7.
Примеры решения задач
| Задание | Элемент образует с водородом газообразное соединение, содержащее 12,5% водорода. Высший оксид этого элемента имеет формулу RO2. Укажите число электронов в электронной оболочке атома этого элемента. |
| Решение | Высшие оксиды составаRO2 образуют элементы, расположенные в IV группе Периодической таблицы. Элементы этой группы образуют с водородом летучие соединения состава RH4.Обозначим искомый элемент как Х. Тогда его массовая доля в составе водородного соединения равна:
ω(Х)=100 – 12,5 = 87,5%. Найдем относительную атомную массу этого элемента: Ar(Х) = ω(Х)× n(H)/ω(Н) = 87,5×4/12,5 = 28. Такую атомную массу имеет кремний (Si). Формулы соединений, указанных в условии задачи, будут выглядеть следующим образом: SiO2и SiH4. Общее число электронов в электронной оболочке атома кремния равно его порядковому номеру в Периодической системе, т.е. 14. |
| Ответ | Общее число электронов в электронной оболочке атома кремния равно 14. |
| Задание | Ядро атома элемента IV периода содержит одинаковое количество протонов и нейтронов. Укажите число атомов в молекуле летучего водородного соединения элемента. |
| Ответ | Число нейтронов в атоме химического элемента определяется как разность между массовым числом и зарядом ядра (M-Z). В IV периоде имеется всего один элемент, у которого число протонов равно числу электронов – это кальций (M=40, Z=20, n=M-Z = 40-20 =20).
Кальций образует с водородом летучих соединений не образует. |











