Гидролиз сложных эфиров
Общие понятия о гидролизе сложных эфиров
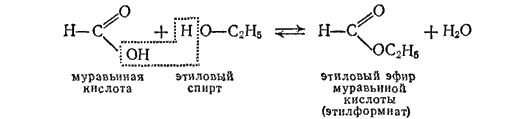
Структурная формула сложных эфиров в общем виде:
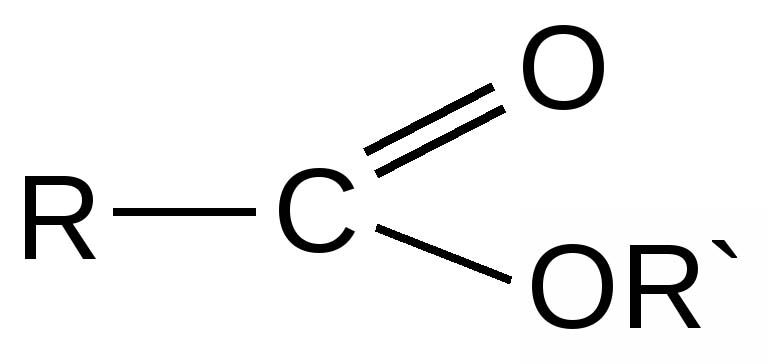
где R и R’ – углеводородные радикалы.
Гидролиз сложных эфиров
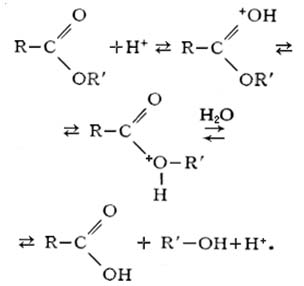
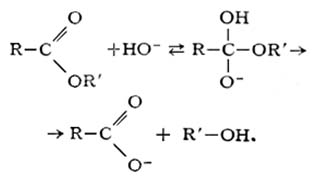
Одной из наиболее характерных для сложных эфиров способностей (помимо этерификации) является их гидролиз – расщепление под действием воды. По-другому гидролиз сложных эфиров называют омылением. В отличие от гидролиза солей в данном случае он практически необратим. Различают щелочной и кислотный гидролиз сложных эфиров. В обоих случаях образуются спирт и кислота:
а) кислотный гидролиз
б) щелочной гидролиз
Примеры решения задач
| Задание | Определите массу уксусной кислоты, которую можно получить в ходе реакции омыления этилацетата массой 180 г. |
| Решение | Запишем уравнение реакции гидролиза этилового эфира уксусной кислоты используя брутто формулы:
C4H8O2 + H2O ↔ CH3COOH + C2H5OH. Рассчитаем количество вещества этилацетата (молярная масса – 88 г/моль), используя значение массы из условий задачи: υ = m/M; υ (C4H8O2) =m (C4H8O2)/M (C4H8O2) = 180/88 = 2 моль. Согласно уравнению реакции, число моль этилацетата и уксусной кислоты равны: υ (C4H8O2) = υ (CH3COOH) = 2моль. Тогда, можно определить массу уксусной кислоты (молярная масса – 60 г/моль): m(CH3COOH)= υ (CH3COOH) × M (CH3COOH) = 2 × 60 = 120г. |
| Ответ | Масса уксусной кислоты 120 грамм. |
| Задание | Напишите уравнение гидролиза малонового эфира. |
| Решение | Малоновый эфир или диэтилмалонат – это эфир двухосновной малоновой кислоты. При его омылении образуется эта кислота и этанол:
C2H5OCO-CH2-COOC2H5 + H2O ↔ НООС-СН₂-СООН + C2H5OH. |











