Гидролиз нитрита калия
Общие сведения о гидролизе нитрита калия

Рис. 1. Нитрит калия. Внешний вид.
В сухом состоянии устойчив на воздухе, во влажном – окисляется кислородом воздуха. На свету частично разлагается и желтеет. Брутто-формула – KNO2. Молярная масса нитрита натрия равна 85,10 г/моль. Молекула имеет строение:
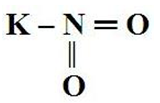
Очень хорошо растворяется в воде (гидролизуется по аниону). Кристаллогидратов не образует. В ОВР может проявлять как окислительные, так и восстановительные свойства.
Гидролиз нитрита калия
Нитрит калия представляет собой среднюю соль, образованную слабой кислотой – азотистой (HNO2) и сильным основанием – гидроксидом калия (KOH):
NaNO2 ↔ K+ + NO2—.
Подвергается гидролизу по аниону. Характер среды водного раствора нитрита натрия – щелочной. Уравнение гидролиза будет выглядеть следующим образом:
K+ + NO2—+ H2O ↔ HNO2 + K+ + OH— (полное ионное уравнение);
NO2—+ H2O ↔ HNO2 + OH— (сокращенное ионное уравнение);
KNO2+ H2O ↔ HNO2 + KOH (молекулярное уравнение).
Примеры решения задач
| Задание | Какова будет реакция среды (кислая или щелочная в растворах следующих солей: а) AgNO3; б) K2CO3; в) KHCO3; г)ZnSO4? Ответ поясните. |
| Ответ | а) нитрат серебра представляет собой соль, образованную сильной кислотой (азотной) и сильным основанием (гидроксидом серебра (I) ):
AgNO3↔ Ag+ +NO3—. Она не подвергается гидролизу. Реакция среды водного раствора нитрата серебра будет нейтральная. б) карбонат калия представляет собой соль, образованную слабой кислотой (угольной) и сильным основанием (гидроксидом калия). Гидролиз протекает по аниону: K2СO3↔ 2K+ +СO32-, СO32- + HOH↔HCO3— + OH—. Наличие гидроксид-ионов свидетельствует о том, что реакция среды водного раствора карбоната калия щелочная. в) гидрокарбонат калия представляет собой соль, образованную слабой кислотой (угольной) и сильным основанием (гидроксидом калия). Гидролиз протекает по аниону: KHСO3 ↔ K+ + HСO3—, HСO3— + HOH ↔ H2CO3 + OH—. Наличие гидроксид-ионов свидетельствует о том, что реакция среды водного раствора гидрокарбоната калия щелочная. г) сульфат цинка представляет собой соль, образованную сильной кислотой (серной) и слабым основанием (гидроксидом цинка). Гидролиз протекает по катиону: ZnSO4 ↔ Zn2+ + SO42-, Zn2+ + HOH ↔ ZnOH+ + H+. Наличие ионов водорода свидетельствует о том, что реакция среды водного раствора сульфата цинка кислая. |
| Задание | Установите соответствие между названием соли и характером среды её водного раствора. Ответ обоснуйте.
|
||||||||||||
| Ответ | Соль хлорид цинка (ZnCl2) образована слабым основанием – гидроксидом цинка (I) и сильной кислотой – соляной (хлороводородной). Подвергается гидролизу по катиону, следовательно, среда кислая (3).
Соль нитрат алюминия (Al(NO3)3) образована слабым основанием – гидроксидом алюминия и сильной кислотой – азотной. Подвергается гидролизу по катиону, следовательно, среда кислая (3). Соль сульфит цинка (ZnSO3) образована слабой кислотой – сернистой и слабым основанием – гидроксидом цинка. Подвергается гидролизу по катиону и аниону, следовательно, среда нейтральная (1). Соль карбонат калия (K2CO3) образована слабой кислотой – угольной и сильным основанием – гидроксидом калия. Подвергается гидролизу по аниону, следовательно, среда щелочная (2). |











