Физические и химические свойства бензола
Формула – С6Н6 (структурная формула – рис. 1). Молекулярная масса – 78, 11.
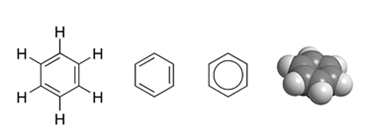
Рис. 1. Структурные и пространственная формулы бензола.
Все шесть атомов углерода в молекуле бензола находятся в sp2 гибридном состоянии. Каждый атом углерода образует 3σ-связи с двумя другими атомами углерода и одним атомом водорода, лежащие в одной плоскости. Шесть атомов углерода образуют правильный шестиугольник (σ-скелет молекулы бензола). Каждый атом углерода имеет одну негибридизованную р-орбиталь, на которой находится один электрон. Шесть р-электронов образуют единое π-электронное облако (ароматическую систему), которое изображают кружочком внутри шестичленного цикла. Углеводородный радикал, полученный от бензола носит название C6H5 – — фенил (Ph-).
Химические свойства бензола
Для бензола характерны реакции замещения, протекающие по электрофильному механизму:
— галогенирование (бензол взаимодействует с хлором и бромом в присутствии катализаторов – безводных AlCl3, FeCl3, AlBr3)
C6H6 + Cl2 = C6H5-Cl + HCl;
— нитрование (бензол легко реагирует с нитрующей смесью – смесь концентрированных азотной и серной кислот)
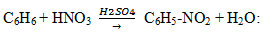
— алкилирование по Фридею-Крафтсу
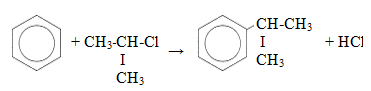
— алкилирование алкенами
C6H6+ CH2 = CH-CH3 → C6H5-CH(CH3)2;
Реакции присоединения к бензолу приводят к разрушению ароматической системы и протекают только в жестких условиях:
— гидрирование (реакция протекает при нагревании, катализатор – Pt)
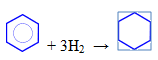
— присоединение хлора (протекает под действием УФ-излучения с образованием твердого продукта – гексахлорциклогексана (гексахлорана) – C6H6Cl6)
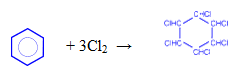
Как и любое органическое соединение бензол вступает в реакцию горения с образованием в качестве продуктов реакции углекислого газа и воды (горит коптящим пламенем):
2C6H6 +15O2 → 12CO2 + 6H2O.
Физические свойства бензола
Бензол – жидкость без цвета, но обладающая специфическим резким запахом. Образует с водой азеотропную смесь, хорошо смешивается с эфирами, бензином и различными органическими растворителями. Температура кипения – 80,1![]() С, плавления – 5,5
С, плавления – 5,5![]() С. Токсичен, канцероген (т.е. способствует развитию онкологических заболеваний).
С. Токсичен, канцероген (т.е. способствует развитию онкологических заболеваний).
Получение и применение бензола
Основные способы получения бензола:
— дегидроциклизация гексана (катализаторы – Pt, Cr3O2)
CH3 –(CH2)4-CH3 → С6Н6 + 4H2↑;
— дегидрирование циклогексана (реакция протекает при нагревании, катализатор – Pt)
С6Н12 → С6Н6 + 4H2↑;
— тримеризация ацетилена (реакция протекает при нагревании до 600![]() С, катализатор – активированный уголь)
С, катализатор – активированный уголь)
3HC≡CH → C6H6.
Бензол служит сырьем для производства гомологов (этилбензола, кумола), циклогексана, нитробензола, хлорбензола и др. веществ. Ранее бензол использовали в качестве присадки к бензину для повышения его октанового числа, однако, сейчас, в связи с его высокой токсичностью содержание бензола в топливе строго нормируется. Иногда бензол используют в качестве растворителя.
Примеры решения задач
| Задание | Запишите уравнения, с помощью которых можно осуществить следующие превращения: CH4 → C2H2 → C6H6 → C6H5Cl. |
| Решение |
Для получения ацетилена из метана используют следующую реакцию:
2CH4 → C2H2 + 3Н2↑ (t
Получение бензола из ацетилена возможно по реакции тримеризации ацетилена, протекающей при нагревании (t 3C2H2 → C6H6. Реакция хлорирования бензола с получением в качестве продукта хлорбензола осуществляется в присутствии хлорида железа (III): C6H6 + Cl2 → C6H5Cl + HCl. |
| Задание | К 39 г бензола в присутствии хлорида железа (III) добавили 1 моль бромной воды. Какое количество вещества и сколько граммов каких продуктов при этом получилось? |
| Решение |
Запишем уравнение реакции бромирования бензола в присутствии хлорида железа (III):
C6H6 + Br2 → C6H5Br + HBr. Продуктами реакции являются бромбензол и бромоводород. Молярная масса бензола, рассчитанная с использованием таблицы химических элементов Д.И. Менделеева – 78 г/моль. Найдем количество вещества бензола: n(C6H6) = m(C6H6) / M(C6H6); n(C6H6) = 39 / 78 = 0,5 моль. По условию задачи бензол вступил в реакцию с 1 моль брома. Следовательно, бензол находится в недостатке и дальнейшие расчеты будем производить по бензолу. Согласно уравнению реакции n(C6H6): n(C6H5Br) : n(HBr) = 1:1:1, следовательно n(C6H6) = n(C6H5Br) = : n(HBr) = 0,5 моль. Тогда, массы бромбензола и бромоводорода будут равны: m(C6H5Br) = n(C6H5Br)×M(C6H5Br); m(HBr) = n(HBr)×M(HBr). Молярные массы бромбензола и бромоводорода, рассчитанные с использованием таблицы химических элементов Д.И. Менделеева – 157 и 81 г/моль, соответственно. m(C6H5Br) = 0,5×157 = 78,5 г; m(HBr) = 0,5×81 = 40,5 г. |
| Ответ | Продуктами реакции являются бромбензол и бромоводород. Массы бромбензола и бромоводорода – 78,5 и 40,5 г, соответственно. |











