Давление газа на стенки сосуда. Закон Дальтона
Давление газа на стенки сосуда
Вследствие теплового движения частицы газа время от времени ударяются о стенки сосуда (рис.1,а). При каждом ударе молекулы действуют на стенку сосуда с некоторой силой. Складываясь друг другом, силы ударов отдельных частиц, образуют некоторую силу давления, постоянно действующую на стенку сосуда. Молекулы газа при столкновениях со стенками сосуда взаимодействуют с ними по законам механики как упругие тела и передают свои импульсы стенкам сосуда (рис.1,б).
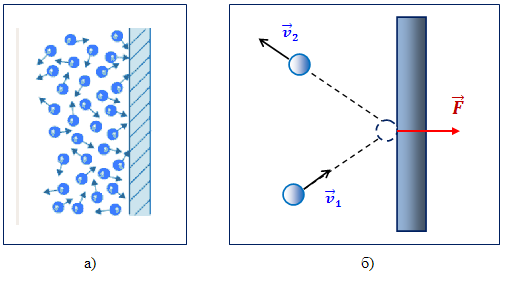
Рис.1. Давление газа на стенку сосуда: а) возникновение давления вследствие ударов о стенку хаотически движущихся частиц; б) сила давления как результат упругого удара частиц.
На практике чаще всего имеют дело не с чистым газом, а со смесью газов. Например, атмосферный воздух представляет собой смесь азота, кислорода, углекислого газа, водорода и других газов. Каждый из газов, входящих в состав смеси, вносит свой вклад в суммарное давление, которое оказывает смесь газов на стенки сосуда.
Закон Дальтона для газовой смеси
Для газовой смеси справедлив закон Дальтона:
давление газовой смеси равно сумме парциальных давлений каждого компонента смеси:
![]()
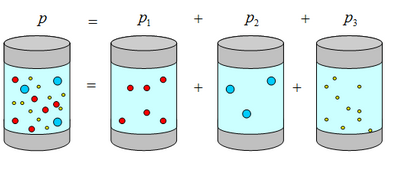
Рис.2. Закон Дальтона для газовой смеси
С точки зрения молекулярно-кинетической теории закон Дальтона выполняется потому, что взаимодействие между молекулами идеального газа пренебрежимо мало. Поэтому каждый газ оказывает на стенку сосуда давление, как если бы остальных газов в сосуде не было.
Примеры решения задач
| Задание | Идеальный газ, находящийся в закрытом сосуде, оказывает давление на его стенки. Это объясняется тем что:
1) молекулы прилипают к стенкам сосуда; 2) идеальный газ имеет большую плотность; 3) молекулы газа передают стенкам энергию; 4) молекулы газа передают стенкам импульс. |
| Ответ | Идеальный газ оказывает давление на стенки сосуда потому, что молекулы газа. ударяясь о стенку сосуда, передают ей свой импульс. Правильный ответ 4). |
| Задание | В закрытом сосуде находится смесь 1 моля кислорода |
| Ответ | Давление газа обусловлено ударами молекул о стенки сосуда, оно не зависит от вида газа. В условиях теплового равновесия температура газов, входящих в состав газовой смеси, в данном случае кислорода и водорода, одинакова. Это значит, что парциальные давления газов зависят от количества молекул соответствующего газа. В одном моле любого вещества содержится |











