Общие формулы углеводородов
Определение и общие формулы углеводородов
К углеводородам относится обширная группа органических соединений. Однако, лишь единственное из них – метан – содержит атом углерода, остальные имеют в своем составе связанные друг с другом атомы углерода, начиная с двух (этана, этилен, ацетилен) и кончая сотнями тысяч в высокомолекулярных углеводородах.
В соответствии со строением углеродного скелета углеводорода делятся на алифатические (с открытой углеродной цепью) и циклические (с замкнутой углеводородной цепью).
В зависимости от типа связей между атомами углерода алифатические углеводороды делятся на насыщенные, содержащие только s-связи и ненасыщенные, содержащие как s-, так и p-связи. К насыщенным углеводородам принадлежат алканы. Ненасыщенные углеводороды в зависимости от характера кратной связи подразделяются на алкены (с двойной связью) и алкины (с тройной связью). Кроме этого, выделяются отдельные группы по числу кратных связей в молекуле, например алкадиены (с двумя двойными связями).
Общая формула гомологического ряда алканов CnH2n+2. Представители алканов: метан (CH4), этан (C2H6), пропан (C3H8), бутан (C4H10) и др.
Общая формула гомологического ряда алкенов CnH2n. Представители алкенов: этилен (C2H4), пропен (C3H6), бутен (C4H8) и др.
Алкадиенами называются ненасыщенные углеводороды, молекулы которых содержат две двойные связи. Общая формула гомологического ряда алкадиенов CnH2n-2. Представители алкадиенов: пропадиен-1,2 (C3H4), бутадиен-1,4 (C4H6) и др.
Общая формула гомологического ряда алкинов CnH2n — 2. Представители алкинов: ацетилен (C2H2), пропин-1 (C3H4), бутин-1 (C4H6) и др.
Циклические углеводороды также как и алифатические могут иметь насыщенный и ненасыщенный характер, кроме этого циклические углеводороды делятся на алициклические и ароматические.
Насыщенные и ненасыщенные карбоциклические углеводороды, объединяют общим названием алициклические, подчеркивая приставкой али- их сходство с алифатическими углеводородами.
Насыщенные алициклические углеводороды называют циклоалканами (общая формула CnH2n, представители – циклопропан, циклобутан, циклопентан и др.), ненасыщенные с одной двойной связью – циклоалкенами, с двумя двойными связями – циклоалкадиенами. Известны алициклические углеводороды и с тройной связью, как правило, в макроцикле.
Среди ароматических соединений наибольшее значение имеют вещества, в молекулах которых содержится одно или несколько бензольных колец (рис. 1). Структурным родоначальником этих веществ служит углеводород бензол C6H6. Углеводороды этого ряда носят общее называние – арены, а их общая формула — CnH2n – 6.
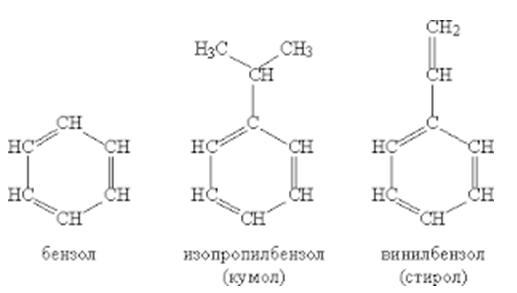
Рис. 1. Ароматические углеводороды.
Примеры решения задач
| Задание | При полном сгорании кислородсодержащего органического вещества массой 13,8 г получили 26,4 г углекислого газа и 16,2 г воды. Найдите молекулярную формулу вещества, если относительная плотность его паров по водороду равна 23. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz+ Oz→CO2 + H2O. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]×M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. Тогда, m(C) = [26,4 / 44]×12 = 7,2 г; m(H) = 2×16,2 / 18 ×1= 1,8 г. m(O) = m(CxHyOz) – m(C) – m(H) = 13,8 – 7,2 – 1,8 = 4,8 г. Определим химическую формулу соединения: x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O); x:y:z= 7,2/12 :1,8/1 :4,8/16; x:y:z= 0,6 : 1,8 : 0,3 = 2: 6 : 1. Значит простейшая формула соединения C2H6O и молярную массу 46 г/моль [M(C2H6O) = 2×Ar(C) + 6×Ar(H) + Ar(O) = 2×12 + 6×1 + 16 = 24 + 6 + 16 = 46 / моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по водороду: Msubstance = M(H2) × D(H2); Msubstance = 2 × 23 = 46 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(C2H6O) = 46 / 46 = 1. Значит формула органического соединения будет иметь вид C2H6O. |
| Ответ | C2H6O |
| Задание | Массовая доля фосфора в одном из его оксидов равна 56,4%. Плотность паров оксида по воздуху равна 7,59. Установите молекулярную формулу оксида. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Вычислим массовую долю кислорода в соединении: ω (O) = 100% — ω(P) = 100% — 56,4% = 43,6%. Обозначим количество моль элементов, входящих в состав соединения за «х» (фосфор), «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y = ω(P)/Ar(P) : ω(O)/Ar(O); x:y= 56,4/31 : 43,6/16; x:y= 1,82 : 2,725= 1 : 1,5 = 2 : 3. Значит простейшая формула соединения фосфора с кислородом будет иметь вид P2O3 и молярную массу 94 г/моль [M(P2O3) = 2×Ar(P) + 3×Ar(O) = 2×31+ 3×16 = 62 + 32 = 94 г/моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по воздуху: Msubstance = Mair × Dair; Msubstance = 29 × 7,59 = 220 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(P2O3) = 220 / 94 = 2. Значит индексы атомов фосфора и кислорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид P4O6. |
| Ответ | P4O6 |











