Формула желтой кровяной соли
Определение и формула желтой кровяной соли
Устойчив на воздухе. Хорошо растворяется в воде. Не реагирует с разбавленными кислотами, щелочами, гидратом аммиака. Слабый восстановитель; окисляется концентрированной азотной кислотой, перманганатом калия, хлором. Вступает в реакции обмена. Реактив на катион Fe3+(образуется синий осадок так называемой берлинской лазури, или турнбулевойсини).

Рис. 1. Желтая кровяная соль. Внешний вид.
Химическая формула желтой кровяной соли
Химическая формула желтой кровяной соли K4[Fe(CN)6]. Она показывает, что в состав данной молекулы входят четыре атома калия (Ar = 39 а.е.м.), один атом железа (Ar = 56 а.е.м.), шесть атомов углерода (Ar = 12а.е.м.) и шесть атомов азота (Ar = 14 а.е.м.). По химической формуле можно вычислить молекулярную массу желтой кровяной соли:
Mr(K4[Fe(CN)6]) = 4×Ar(K) + Ar(Fe) + 6×Ar(C) + 6×Ar(N);
Mr(K4[Fe(CN)6]) = 4×39 + 56 + 6×12 + 6×14 = 156 + 56 + 72 + 84 = 368.
Графическая (структурная) формула желтой кровяной соли
Структурная (графическая) формула желтой кровяной соли является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 2.).
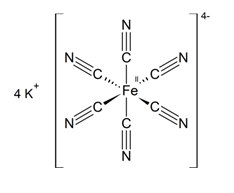
Рис. 2. Структурная формула желтой кровяной соли.
Ионная формула
В водном растворе желтая кровяная соль может диссоциировать согласно следующему уравнению:
K4[Fe(CN)6] ↔ 4K+ + [Fe(CN)6]4-;
[Fe(CN)6]4- ↔ Fe2+ + 6CN—.
Примеры решения задач
| Задание | Массовая доля фосфора в одном из его оксидов равна 56,4%. Плотность паров оксида по воздуху равна 7,59. Установите молекулярную формулу оксида. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Вычислим массовую долю кислорода в соединении: ω (O) = 100% — ω(P) = 100% — 56,4% = 43,6%. Обозначим количество моль элементов, входящих в состав соединения за «х» (фосфор), «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y = ω(P)/Ar(P) : ω(O)/Ar(O); x:y= 56,4/31 : 43,6/16; x:y= 1,82 : 2,725= 1 : 1,5 = 2 : 3. Значит простейшая формула соединения фосфора с кислородом будет иметь вид P2O3 и молярную массу 94 г/моль [M(P2O3) = 2×Ar(P) + 3×Ar(O) = 2×31+ 3×16 = 62 + 32 = 94 г/моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по воздуху: Msubstance = Mair × Dair; Msubstance = 29 × 7,59 = 220 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(P2O3) = 220 / 94 = 2. Значит индексы атомов фосфора и кислорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид P4O6. |
| Ответ | P4O6 |
| Задание | В натуральном жемчуге массовые отношения кальция, углерода и кислорода равны 10:3:12. Какова простейшая формула жемчуга? |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы кальция, углерода и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(C)=12 г/моль, а М(O) = 32 г/моль. Тогда, количество вещества этих элементов равно: n (Ca) = m (Ca) / M (Ca); n (Ca) = 10 / 40 = 0,25 моль. n (C) = m (C) / M (C); n (C) = 3 / 12 = 0,25 моль. n (O) = m (O) / M (O); n (O) = 12 / 16 = 0,75 моль. Найдем мольное отношение: n(Ca) :n(C):n(O) = 0,25 : 0,25 : 0,75= 1 : 1 : 3, т.е. формула соединения жемчуга имеет вид CaCO3. |
| Ответ | CaCO3 |











