Формула хлорной воды
Определение и формула хлорной воды
Получение хлорной воды соответствует следующему уравнению:
Cl2 + H2O = HCl + HClO
Хлорная вода является сильным окислителем. Растворяет золото.
Химическая формула хлорной воды
По сути хлорная вода представляет собой смесь веществ, находящихся в растворе, поэтому укажем химические формулы каждого из них. Химическая формула молекулярного хлора Cl2, хлорной кислоты HClO, хлороводородной (соляной) кислоты HCl. Химическая формула показывает качественные и количественный состав молекулы (сколько и каких атомов присутствует в ней). По химической формуле можно вычислить молекулярную массу вещества:
Mr(Cl2) = 2×Ar(Cl);
Mr(Cl2) = 2×35,5 = 71
Mr(HClO) = Ar(H) + Ar(Cl) + Ar(O);
Mr(HClO) = 1 + 35,5 + 16 =52,5
Mr(HCl) = Ar(H) + Ar(Cl);
Mr(HCl) = 1 + 35,5 = 36,5
Структурная (графическая) формула хлорной воды
Структурная (графическая) формула вещества является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы. Укажем структурные формулы каждого из соединений, водящих в состав хлорной воды.
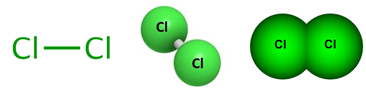
Рис. 1. Структурная формула хлора.
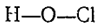
Рис. 2. Структурная формула хлорной кислоты.
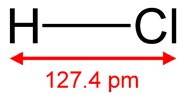
Рис. 3. Структурная формула хлороводородной кислоты.
Ионная формула
Хлороводородная и хлорная кислоты являются электролитами, т.е. способны диссоциировать на ионы в водном растворе согласно следующим уравнениям реакций:
HCl ↔ H+ + Cl—;
HClO ↔ H+ + ClO—
Электронная формула
Электронная формула хлора, показывающая распределение электронов в атоме по энергетическим подуровням показана ниже:
17Cl 1s22s22p63s23p5
Она также показывает, что хлор относится к элементам р-семейства, а также число валентных электронов — на внешнем энергетическом уровне находится 7 электронов (3s23p5).
Электронная формула хлороводородной кислоты показана ниже (рис. 4):
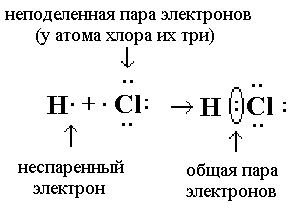
Рис. 4. Электронная формула хлороводородной кислоты.
Примеры решения задач
| Задание | Элементарный состав вещества следующий: массовая доля элемента железа 0,7241 (или 72,41%), массовая доля кислорода 0,2759 (или 27,59%). Выведите химическую формулу. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100% Обозначим число атомов железа в молекуле через «х», число атомов кислорода через «у». Найдем соответствующие относительные атомные массы элементов железа и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(Fe) = 56; Ar(O) = 16 Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y= ω(Fe)/Ar(Fe) : ω(O)/Ar(O); x:y= 72,41/56 : 27,59/16; x:y= 1,29 :1,84 Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 1,29): 1,29/1,29 : 1,84/1,29; 1 : 1,5 = 2 : 3. Следовательно, простейшая формула соединения железа с кислородом имеет вид Fe2O3. |
| Ответ | Fe2O3 |
| Задание | Найдите химическую формулу вещества, в состав которого входит 9 массовых частей алюминия и 8 массовых частей кислорода. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M Найдем молярные массы алюминия и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Al)= 27 г/моль, а М(O) = 16 г/моль. Тогда, количество вещества этих элементов равно: n (Al) = m (Al) / M (Al); n (Al) = 9 / 27 = 0,33моль n (O) = m (O) / M (O); n (O) = 8 / 16 = 0,5 моль Найдем мольное отношение: n(Al) :n(O) = 0,33 : 0,5= 1 : 1,5 = 2 : 3, т.е. формула соединения алюминия с кислородом имеет вид Al2O3. |
| Ответ | Al2O3 |











