Формула углерода
Атомная масса: 12,0107 а.е.м.
Электронная формула углерода
Электронная формула: 1s2 2s2 2p2
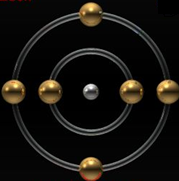
Электронно-графическая формула углерода
Электронно-графическая формула углерода в основном состоянии:

Углерод имеет два неспаренных электрона, проявляет валентность II.
Электронно-графическая формула углерода в возбужденном состоянии:
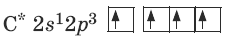
Углерод имеет четыре неспаренных электрона, проявляет валентность IV.
Углерод образует множество аллотропных модификаций, которые очень сильно различаются между собой по внешнему виду, твердости, электропроводности, химической активности и другим свойствам.
Модификации углерода
Среди аллотропных модификаций углерода выделяют кристаллические:
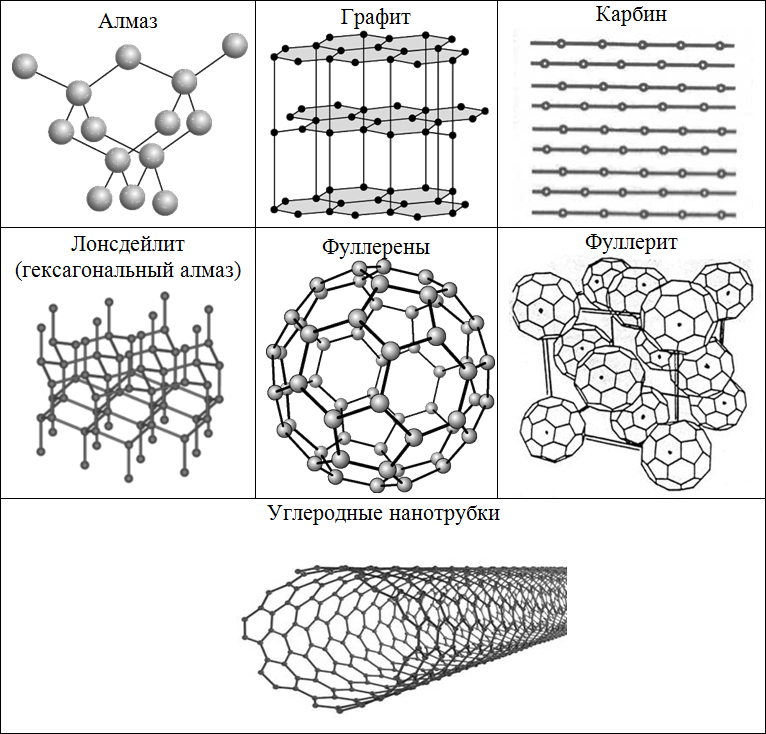
аморфные:

и кластерные формы:

При нормальных условиях термодинамически устойчивым является только графит, а алмаз и другие кристаллические формы – метастабильны.
Большинство аморфных аллотропных форм являются химическими соединениями с высоким содержанием углерода (обычно мелкодисперсного графита), а не чистой аллотропной формой углерода.
Содержание углерода в земной коре составляет 0,023% по массе. Свободный углерод встречается в природе в виде алмаза и графита. Углерод главным образом накапливается в верхней части земной коры, в биосфере. Содержание углерода в живом веществе – 18%,в древесине – 50%, каменном угле – 80%, нефти – 85%, антраците – 96%. Большая часть углерода литосферы сосредоточена в виде карбонатов (известняков и доломитов).
Примеры решения задач
| Задание | Для восстановления 240 г оксида магния потребовалось 80 г угля: Каково процентное содержание чистого углерода в этом угле? |
| Решение | Запишем уравнение реакции:
Найдем количество вещества оксида магния:
По уравнению реакции
Рассчитаем массовую долю углерода в угле: 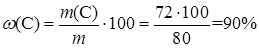
|
| Ответ | В угле содержится 90% углерода. |
| Задание | Вычислите, какой объем метана (н.у.) можно получить из 1 тонны каменного угля, массовое содержание углерода в котором 85 %. Выход реакции получения метана составляет 75 % от теоретически возможного. |
| Решение | Запишем уравнение реакции:
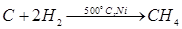
Найдем массу углерода, вступившего в реакцию:
Рассчитаем количество вещества углерода:
По уравнению реакции
Один моль газа при нормальных условиях занимает объем 22,4л. Рассчитаем теоретический объем образовавшегося метана:
Найдем фактический объем образовавшегося метана:
|
| Ответ | Объем образовавшегося метана равен 1190 м |











