Формула сульфата железа 3
Определение и формула сульфата железа 3
Хорошо растворяется в воде (гидролизуется по катиону). Не растворяется в концентрированной серной кислоте. Разлагается горячей водой, щелочами, гидратом аммиака. В ОВР проявляет свойства слабого окислителя. Вступает в реакции обмена.

Рис. 1. Сульфат железа (III). Внешний вид.
Химическая формула сульфата железа 3
Химическая формула сульфата железа (III) Fe2(SO4)3. Она показывает, что в состав данной молекулы входят два атома железа (Ar = 56 а.е.м.), три атома серы (Ar = 32 а.е.м.) и двенадцать атомов кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу сульфата железа (III):
Mr(Fe2(SO4)3) = 2×Ar(Fe) + 3×Ar(S) + 12×Ar(O);
Mr(Fe2(SO4)3) = 2×56 + 3×32 + 12×16 = 112 + 96 + 192 = 400.
Графическая (структурная) формула сульфата железа 3
Структурная (графическая) формула сульфата железа (III) является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
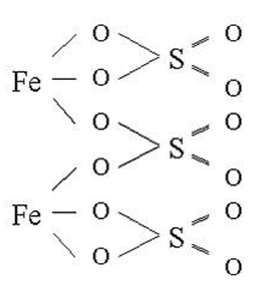
Ионная формула
Сульфат железа (III) является электролитом, т.е. в водном растворе диссоциирует на ионы согласно следующему уравнению:
Fe2(SO4)3 ↔ 2Fe3+ + 3SO42-.
Примеры решения задач
| Задание | При сжигании 24,6 г вещества образовалось 26,88 л углекислого газа (при н.у.), 9 г воды и 2,24 л азота (при н.у.). 1 литр паров этого вещества (н.у.) имеет массу 5,491 г. Установите молекулярную формулу органического вещества. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyNzOw + Oz →CO2 + H2O + N2. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м., Ar(N) = 14 а.е.м. Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. Тогда, m(C) = n(C)×M(C) = n(CO2)×M(C) = [V(CO2) / Vm]×M(C); m(C) = [26,88 / 22,4]×12 = 14,4 г. m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); m(H) = [2×9 / 18]×1 = 1 г. m(N) = n(N)×M(N) = 2×[V(N2) / Vm]; m(N) = 2×[2,24 / 22,4] = 1,28 г. m(O) = m(CxHyNzOw) – m(C) – m(H) – m(N) = 24,6 – 14,4 – 1 – 1,28 = 6,4 г Определим химическую формулу соединения: x:y:z:w = m(C)/Ar(C) : m(H)/Ar(H) : m(N)/Ar(N) : m(O)/Ar(O) x:y:z:w= 14,4/12 : 1/1 : 1,28/14 : 6,4/16; x:y:z:w= 1,2 : 1 : 0,09 : 0,4 = 13 : 11 : 1 : 4. Значит простейшая формула соединения C13H11NO4и молярную массу 30 г/моль [M(C13H11NO4) = 13×Ar(C) + 11×Ar(H) +Ar(N) + 3× Ar(O) = 13×12 + 11×1 + 14 + 3×16 = 156 + 11 + 14 + 48 = 229 г/моль]. Найдем истинную молярную массу органического вещества: M(CxHyNzOw) = m(CxHyNzOw) × Vm/ V(CxHyNzOw); M(CxHyNzOw) = 5491 × 22,4 / 1 = 123 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение истинной и полученной молярных масс: M(CxHyNzOw) / M(C13H11NO4) = 123 / 229 = 0,5. Значит индексы атомов углерода, водорода и кислорода должны быть умножены на 0,5, т.е. формула вещества будет иметь вид C6H5NO2. Это нитробензол. |
| Ответ | C6H5NO2 |
| Задание | Установите массовую формулу вещества, содержащего 33,3% натрия, 20,3% азота и 46,4% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (натрий), «у» (азот) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(Na)/Ar(Na) :ω(N)/Ar(N) : ω(O)/Ar(O); x:y:z= 33,3/23 : 20,3/14 : 46,4/16; x:y:z= 1,45 : 1,45:2,9 = 1 : 1: 2. Значит формула соединения натрия, азота и кислорода будет иметь вид NaNO2. Это нитрит натрия. |
| Ответ | NaNO2 |











