Формула сульфата цинка
Определение и формула сульфата цинка
Хорошо растворяется в воде (гидролизуется по катиону). Реагирует с концентрированной серной кислотой, щелочами, гидратом аммиака. Вступает в реакции обмена и комплексообразования.

Рис. 1. Сульфат цинка. Внешний вид.
Химическая формула сульфата цинка
Химическая формула сульфата цинка имеет вид ZnSO4. Она показывает, что в состав данной молекулы входят один атом цинка (Ar = 65 а.е.м.), один атом серы (Ar = 32 а.е.м.) и четыре атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу сульфата цинка:
Mr(ZnSO4) = Ar(Zn) + Ar(S) + 4×Ar(О);
Mr(ZnSO4) = 65 + 32 + 4×16 = 65 + 32 + 64 = 161.
Графическая (структурная) формула сульфата цинка
Структурная (графическая) формула является более наглядной, она отражает то, как атомы связаны между собой внутри молекулы сульфата цинка (рис. 2).
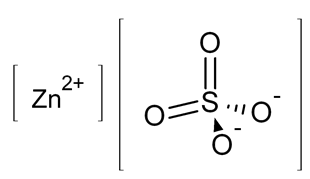
Рис. 2. Графическая формула сульфата цинка.
Ионная формула
Сульфат цинка – электролит. В водном растворе под действием электрического тока он частично диссоциирует на ионы согласно следующему уравнению:
ZnSO4↔Zn2+ + SO42-.
Примеры решения задач
| Задание | Определите состав английской (горькой) соли, используемой медиками, если она содержит 9,86% магния, 13,01% серы, 71,40% кислорода и 5,73% водорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов магния в молекуле через «х», серы — «у», кислорода – «z» и водорода «w». Найдем соответствующие относительные атомные массы элементов магния, серы, кислорода и водорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(Mg) = 24; Ar(H) = 1; Ar(S) = 32; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y:z:w= ω(Mg)/Ar(Mg) : ω(S)/Ar(S) : ω(O)/Ar(O) : ω(H)/Ar(H); x:y:z:w= 9,86%/24 : 13,01%/32 : 71,40%/16 : 5,73%/1; x:y:z:w= 0,41 : 0,41 : 4,46 : 5,73; Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,41): 1 : 1 : 11 : 14. Следовательно, простейшая формула соединения магния, серы, кислорода и водорода имеет вид MgSO11H14. |
| Ответ | MgSO11H14 |
| Задание | Фторотан, применяемый в медицине для наркоза, относится к классу галогенпроизводных и имеет относительную молекулярную массу 197,5. Элементарный состав его в массовых долях: С – 12,2%; Н – 0,51%; Br – 40,4%; F – 28,9%; Cl – 18,0%. Выведите эмпирическую формулу фторотана. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов углерода в молекуле через «х», водорода — «у», брома – «z», фтора — «w» и хлора «k» (CxHyBrzFwClk). Найдем соответствующие относительные атомные массы элементов углерода, водорода, брома, фтора и хлора (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(С) = 12; Ar(H) = 1; Ar(Br) = 80; Ar(F) = 19; Ar(Cl) = 35,5. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y:z:w:k= ω(C)/Ar(C) : ω(H)/Ar(H) : ω(Br)/Ar(Br) : ω(F)/Ar(F): ω(Cl)/Ar(Cl); x:y:z:w:k= 12,2/12 : 0,51/1 : 40,4/80 : 28,9/19: 18,0/35,5; x:y:z:w:k = 1 : 0,51 : 0,5 : 1,5 : 0,5; Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,5): 2 : 1 : 1 : 3 : 1. Следовательно, простейшая формула соединения углерода, водорода, брома, фтора и хлора имеет вид C2HBrF3Cl, а молярная масса 197,5 г/моль [M(C2HBrF3Cl) = 2×Ar(C) + Ar(H) + Ar(Br) + 3×Ar(F) + Ar(Cl) = 2×12 + 1 + 80 + 3×19 + 35,5 = 24 + 81 + 57 + 35,5 =197,5 г/моль]. Чтобы найти эмпирическую (истинную) формулу фторотана найдем отношение молярных масс (полученной и указанной в условии задачи): Msubstance / M(C2HBrF3Cl) = 197,5 / 197,5 = 1. Значит эмпирическая формула фторотана имеет вид C2HBrF3Cl. |
| Ответ | C2HBrF3Cl |











