Формула сероводородной кислоты
Определение и формула сероводородной кислоты
Термически неустойчив. Плохо растворим в холодной воде. Насыщенный раствор (0,1М) называют «сероводородной водой», который мутнеет при стоянии на воздухе. Проявляет слабые кислотные свойства. В ОВР является сильным восстановителем.
Химическая формула сероводородной кислоты
Химическая формула сероводородной кислоты H2S. Она показывает, что в состав данной молекулы входят два атома водорода (Ar = 1 а.е.м.) и один атом серы (Ar = 32 а.е.м.). По химической формуле можно вычислить молекулярную массу сероводородной кислоты:
Mr(H2S) = 2×Ar(H) + Ar(S);
Mr(H2S) = 2×1 + 32 = 2 +32 = 34.
Графическая (структурная) формула сероводородной кислоты
Структурная (графическая) формула сероводородной кислоты является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 1).
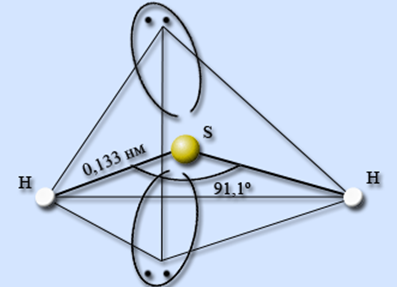
Рис. 1. Строение молекулы сероводорода с указанием валентного угла между связями и длины химических связей.
Ионная формула
Сероводородная кислота является электролитом, т.е. в водном растворе она способна диссоциировать на ионы согласно следующему уравнению:
H2S ↔ 2H+ + S2-.
Примеры решения задач
| Задание | Определите молекулярную формулу соединения, содержащего 49,4% калия, 20,2% серы, 30,4% кислорода, если относительная молекулярная масса этого соединения в 3,95 раза больше относительной атомной массы кальция. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (сера) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(K)/Ar(K) : ω(S)/Ar(S) : ω(O)/Ar(O); x:y:z= 49,4/39 : 20,2/32 : 30,4/16; x:y:z= 1,3 : 0,63:1,9 = 2 : 1: 3. Значит простейшая формула соединения калия, серы и кислорода будет иметь вид K2SO3 и молярную массу 158 г/моль[M(K2SO3) = 2×Ar(K) + Ar(S) + 3×Ar(O) = 2×39 + 32 + 3×16 = 78 + 32 + 48 = 158 г/моль]. Найдем истинную молярную массу этого соединения: Msubstance = Ar(Ca) × 3,95 = 40 × 3,95 = 158 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(K2SO3) = 158 / 158 = 1. Значит формула соединения калия, серы и кислорода имеет вид K2SO3. |
| Ответ | K2SO3 |
| Задание | В состав вещества входит 32,5% натрия, 22,5% серы и 45% кислорода. Выведите химическую формулу вещества. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (натрий), «у» (сера) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(Na)/Ar(Na) : ω(S)/Ar(S) : ω(O)/Ar(O); x:y:z= 32,5/23 : 22,5/32 : 45/16; x:y:z= 1,4 : 0,7: 2,8 = 2 : 1: 4. Значит формула соединения натрия, серы и кислорода будет иметь вид Na2SO4. Это сульфат натрия. |
| Ответ | Na2SO4 |











