Формула сернистой кислоты
Определение и формула сернистой кислоты
Существует в водном растворе только при концентрации не более 6%, в остальных случаях сразу же разлагается на диоксид серы и воду. Плотность – 1,03 г/см3.
Химическая формула сернистой кислоты
Химическая формула сернистой кислоты H2SO3. Она показывает, что в состав данной молекулы входят два атома водорода (Ar = 1 а.е.м.), один атом серы (Ar = 32 а.е.м.) и три атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу сернистой кислоты:
Mr(H2SO3) = 2×Ar(H) + Ar(S) + 3×Ar(O);
Mr(H2SO3) = 2×1 + 32 + 3×16= 2 + 32 + 48 = 82
Графическая (структурная) формула сернистой кислоты
Структурная (графическая) формула сернистой кислоты является более наглядной (рис. 1). Она показывает то, как связаны атомы между собой внутри молекулы:
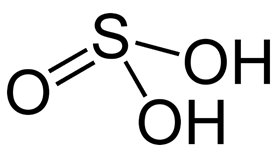
Рис. 1. Структурная формула сернистой кислоты.
Ионная формула
Сернистая кислота представляет собой двухосновную кислоту, которая подвергается ступенчатой диссоциации в водном растворе согласно следующим уравнениям реакции:
H2SO3 ↔ H+ + HSO3—;
HSO3— ↔ H+ + SO32-
Примеры решения задач
| Задание | При сжигании 6,5 г газообразного органического соединения получено 11,2 л (н.у.) углекислого газа и 4,5 г воды. Относительная плотность этого соединения по водороду равна 13. Выведите его химическую формулу. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz →CO2 + H2O Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(CO2) = [V(CO2) / Vm]×M(CO2); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×n(H2O) / M(H2O)]×M(H) Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль Тогда, m(C) = [11,2 / 22,4]×44 = 6 г; m(H) = [2×4,5 / 18] ×1 = 0,5 г m(O) = m(CxHyOz) – m(C) – m(H) = 6,5 – 6 – 0,5 = 0, что свидетельствует о том, что в составе данного органического вещества нет. Определим химическую формулу соединения как CxHy: x:y = m(C)/Ar(C) : m(H)/Ar(H); x:y =6/12 :0,5/1; x:y = 0,5 : 0,5 = 1: 1 Значит простейшая формула соединения CH и молярную массу 13 г/моль [M(CH) = Ar(C) + Ar(H)= 12 + 1 = 13 г/моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по водороду: Msubstance = M(H2) × D(H2); Msubstance = 2 × 13 = 26 г/моль Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(CH) = 26 / 13 = 2 Значит индексы атомов углерода и водорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид C2H2. Это ацетилен. |
| Ответ | C2H2 |
| Задание | В результате сгорания кислородсодержащего органического соединения в избытке воздуха собрано 1,584 г углекислого газа и 0,972 мл воды. Плотность пара этого соединения по воздуху равна 1,5865. Выведите химическую формулу соединения, если она содержит два одноименных радикала. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz+ Oz→CO2 + H2O Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]/M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); m(H) =[2×V(H2O)×M(H) / M(H2O)×1 (г/мл)] Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль Тогда, m(C) = [1,584 / 44]/12 = 0,432 г; m(H) = [2×0,971 ×1 / 18 ×1 (г/мл)] = 0,108 г Значение молярной массы органического вещества можно определить при помощи его плотности по воздуху: Msubstance = Mair × Dair; Msubstance = 29 × 1,5862 = 46 г/моль Найдем число атомов углерода и водорода в соединении: x:y = m(C)/Ar(C) : m(H)/Ar(H); x:y = 0,432/12 :0,108/1; x:y = 0,036 : 0,108 = 1: 3 Значит простейшая формула углеводородного радикала этого соединения имеет вид CH3и молярную массу 15 г/моль [M(CH) = Ar(C) + 3×Ar(H)= 12 + 3×1 = 12 + 3 = 15 г/моль]. Это означает, что на кислород приходится [46-15 = 31 г/моль], что невозможно. Учитывая условие задачи про два одноименных радикала 2×М(CH3) = 2×15 = 30 г/моль, получаем, что на кислород приходится [46-30 = 16 г/моль], т.е. органическое кислородсодержащее соединение имеет вид CH3-O-CH3. Это ацетон (диметилкетон). |
| Ответ | CH3-O-CH3 |











