Формула ртути
Определение и формула ртути
Очень легкоплавкий металл. Плотность 13,55 г/см3. Температура плавления — 38,9oC, кипения 357oC.

Рис. 1. Ртуть. Внешний вид.
Химическая формула ртути
Химическое обозначение ртути – Hg от латинского слова «hydrargyrum». Этот химический элемент расположен в шестом периоде II группе побочной (В) подгруппе Периодической таблицы. Относится к элементамd-семейства. Металл. Относительная атомная масса ртути равна 200,59 а.е.м.
Электронная формула ртути
Атом ртути состоит из положительно заряженного ядра (+80), внутри которого есть 80 протонов и 120 нейтронов, а вокруг, по шести орбитам движутся 80 электронов.
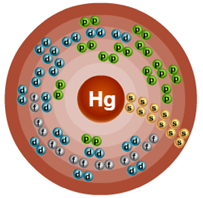
Рис. 2. Схематическое строение атома ртути.
Распределение электронов по орбиталям выглядит следующим образом:
+80 Hg)2)8)18)32)18)2;
1s22s22p63s23p63d104s24p64f145s25p65d106s2.
Примеры решения задач
| Задание | Элементарный состав вещества следующий: массовая доля элемента железа 0,7241 (или 72,41%), массовая доля кислорода 0,2759 (или 27,59%). Выведите химическую формулу. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100% Обозначим число атомов железа в молекуле через «х», число атомов кислорода через «у». Найдем соответствующие относительные атомные массы элементов железа и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(Fe) = 56; Ar(O) = 16 Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y= ω(Fe)/Ar(Fe) : ω(O)/Ar(O); x:y = 72,41/56 : 27,59/16; x:y = 1,29 : 1,84 Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 1,29): 1,29/1,29 : 1,84/1,29; 1 : 1,5 = 2 : 3. Следовательно, простейшая формула соединения железа с кислородом имеет вид Fe2O3. |
| Ответ | Fe2O3 |
| Задание | Найдите химическую формулу вещества, в состав которого входит 9 массовых частей алюминия и 8 массовых частей кислорода. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M Найдем молярные массы алюминия и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Al)= 27 г/моль, а М(O) = 16 г/моль. Тогда, количество вещества этих элементов равно: n (Al) = m (Al) / M (Al); n (Al) = 9 / 27 = 0,33моль n (O) = m (O) / M (O); n (O) = 8 / 16 = 0,5 моль Найдем мольное отношение: n(Al) :n(O) = 0,33 : 0,5= 1 : 1,5 = 2 : 3, т.е. формула соединения алюминия с кислородом имеет вид Al2O3. |
| Ответ | Al2O3 |











