Формула оксида железа
Определение и формула оксида железа
Железо образует два оксида, в которых проявляет валентности II и III и степени окисления (+2) и (+3) соответственно.
После прокаливания химически неактивен. В виде порошка пирофорен. Не реагирует с холодной водой. Проявляет амфотерные свойства (с преобладанием основных). Легко окисляется кислородом. Восстанавливается водородом и углеродом.

Рис. 1. Оксид железа (II). Внешний вид.
Термически устойчив. Температура плавления 1562oC.

Рис. 1. Оксид железа (III).
Не реагирует с водой, гидратом аммиака. Проявляет амфотерные свойства, реагирует с кислотами, щелочами. Восстанавливается водородом, монооксидом углерода, железом.
Химическая формула оксида железа
Химическая формула оксида железа (II) FeO, а оксида железа (III) — Fe2O3. Химическая формула показывает качественные и количественный состав молекулы (сколько и каких атомов присутствует в ней). По химической формуле можно вычислить молекулярную массу вещества (Ar(Fe) = 56 а.е.м., Ar(O) = 16 а.е.м.):
Mr(FeO) = Ar(Fe) + Ar(O);
Mr(FeO) = 56 + 16 = 72.
Mr(Fe2O3) = 2×Ar(Fe) + 3×Ar(O);
Mr(Fe2O3) = 2×56 + 3×16 = 58 + 48 = 160.
Структурная (графическая) формула оксида железа
Структурная (графическая) формула вещества является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы. Ниже представлены графические формулы оксидов железа (а – FeO, б — Fe2O3):
а)
Fe = O;
б)
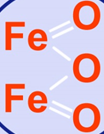
Примеры решения задач
| Задание | Подвергнув анализу вещество, установили, что в его состав входят: натрий с массовой долей 0,4207 (или 42,07%), фосфор с массовой долей 0,189 (или 18,91%), кислород с массовой долей 0,3902 (или 39,02%). Найдите формулу соединения. |
| Решение | Обозначим число атомов натрия в молекуле через «х», число атомов фосфора через «у» и число атомов кислорода через «z».
Найдем соответствующие относительные атомные массы элементов натрия, фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(Na) = 23; Ar(P) = 31; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: Na:P:O = 42,07/39 : 18,91/31 : 39,02/16; Na:P:O = 1,829 : 0,61 : 2,43. Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,61): 1,829/0,61 : 0,61/0,61 : 2,43/0,61; 3 : 1: 4. Следовательно, простейшая формула соединения натрия, фосфора и кислорода имеет вид Na3PO4. Это фосфат натрия. |
| Ответ | Na3PO4 |
| Задание | Молярная масса соединения азота с водородом равна 32 г/моль. Определите молекулярную формулу вещества, массовая доля азота в котором составляет 85,7%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Вычислим массовую долю водорода в соединении: ω (H) = 100% — ω(N) = 100% — 85,7% = 14,3%. Обозначим количество моль элементов, входящих в состав соединения за «х» (азот), «у» (водород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y = ω(N)/Ar(N) : ω(H)/Ar(H); x:y= 85,7/14 : 14,3/1; x:y= 6,12 : 14,3= 1 : 2. Значит простейшая формула соединения азота с водородом будет иметь вид NH2 и молярную массу 16 г/моль [M(NH2) = Ar(N) + 2×Ar(H) = 14+ 2×1 = 14 + 2 = 16 г/моль]. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(NH2) = 32 / 16 = 2. Значит индексы атомов азота и водорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид N2H4. Это гидразин. |
| Ответ | N2H4 |











