Формула оксида алюминия
Определение и формула оксида алюминия
Является исходным сырьем для получения алюминия. В природе встречается в виде корунда и его разновидностей. Если бесцветные кристаллы корунда окрашены примесями в голубой цвет, то они называются сапфирами, в фиолетовый – аметистами, в красный – рубинами.

Рис. 1. Оксид алюминия. Внешний вид.
Оксид алюминия не растворяется в воде и с ней не реагирует. Проявляет амфотерные свойства: реагирует с концентрированными кислотами, щелочами в концентрированном растворе и при спекании. В прокаленном виде химически пассивен.
Химическая формула оксида алюминия
Химическая формула оксида алюминия Al2O3. Она показывает, что в состав данной молекулы входят два атома алюминия (Ar = 27 а.е.м.) и три атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу оксида алюминия:
Mr(Al2O3) = 2×Ar(Al) + 3×Ar(O);
Mr(Al2O3) = 2×27 + 3×16 = 54 + 48 = 102
Графическая (структурная) формула оксида алюминия
Структурная (графическая) формула оксида алюминия является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 2).
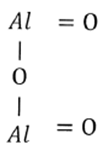
Рис. 2. Графическая формула оксида алюминия.
Примеры решения задач
| Задание | При сжигании 6,5 г газообразного органического соединения получено 11,2 л (н.у.) углекислого газа и 4,5 г воды. Относительная плотность этого соединения по водороду равна 13. Выведите его химическую формулу. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz →CO2 + H2O Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(CO2) = [V(CO2) / Vm]×M(CO2); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×n(H2O) / M(H2O)]×M(H) Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль Тогда, m(C) = [11,2 / 22,4]×44 = 6 г; m(H) = [2×4,5 / 18] ×1 = 0,5 г m(O) = m(CxHyOz) – m(C) – m(H) = 6,5 – 6 – 0,5 = 0, что свидетельствует о том, что в составе данного органического вещества нет. Определим химическую формулу соединения как CxHy: x:y = m(C)/Ar(C) : m(H)/Ar(H); x:y =6/12 :0,5/1; x:y = 0,5 : 0,5 = 1: 1 Значит простейшая формула соединения CH и молярную массу 13 г/моль [M(CH) = Ar(C) + Ar(H)= 12 + 1 = 13 г/моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по водороду: Msubstance = M(H2) × D(H2); Msubstance = 2 × 13 = 26 г/моль Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(CH) = 26 / 13 = 2 Значит индексы атомов углерода и водорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид C2H2. Это ацетилен. |
| Ответ | C2H2 |
| Задание | В результате сгорания кислородсодержащего органического соединения в избытке воздуха собрано 1,584 г углекислого газа и 0,972 мл воды. Плотность пара этого соединения по воздуху равна 1,5865. Выведите химическую формулу соединения, если она содержит два одноименных радикала. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz+ Oz→CO2 + H2O Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]/M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); m(H) =[2×V(H2O)×M(H) / M(H2O)×1 (г/мл)] Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль Тогда, m(C) = [1,584 / 44]/12 = 0,432 г; m(H) = [2×0,971 ×1 / 18 ×1 (г/мл)] = 0,108 г Значение молярной массы органического вещества можно определить при помощи его плотности по воздуху: Msubstance = Mair × Dair; Msubstance = 29 × 1,5862 = 46 г/моль Найдем число атомов углерода и водорода в соединении: x:y = m(C)/Ar(C) : m(H)/Ar(H); x:y = 0,432/12 :0,108/1; x:y = 0,036 : 0,108 = 1: 3 Значит простейшая формула углеводородного радикала этого соединения имеет вид CH3и молярную массу 15 г/моль [M(CH) = Ar(C) + 3×Ar(H)= 12 + 3×1 = 12 + 3 = 15 г/моль]. Это означает, что на кислород приходится [46-15 = 31 г/моль], что невозможно. Учитывая условие задачи про два одноименных радикала 2×М(CH3) = 2×15 = 30 г/моль, получаем, что на кислород приходится [46-30 = 16 г/моль], т.е. органическое кислородсодержащее соединение имеет вид CH3-O-CH3. Это ацетон (диметилкетон). |
| Ответ | CH3-O-CH3 |











