Формула мрамора
Определение и формула мрамора
В обычных условиях он представляет собой белый порошок (рис. 1) разлагающийся при прокаливании и плавящийся без разложения под избыточным давлением углекислого газа. Практически не растворяется в воде, не реагирует со щелочами. Разлагается кислотами, хлоридом аммония в растворе. Переводится в раствор избытком углекислого газа, образуя гидрокарбонат кальция.

Рис.1. Карбонат кальция (основа мрамора). Внешний вид.
Химическая формула мрамора
Химическая формула карбоната кальция – CaCO3. Она показывает, что в составе молекулы этого сложного вещества находится один атома кальция (Ar = 40 а.е.м.), один атом углерода (Ar = 12 а.е.м.)и три атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу карбоната кальция:
Mr(CaCO3) = Ar(Ca) + Ar(C) + 3×Ar(O);
Mr(CaCO3) = 40 + 12 + 3×16 = 52 +48 =100
Структурная (графическая) формула мрамора
Более наглядной является структурная (графическая) формула карбоната кальция. Она показывает то, как связаны атомы между собой внутри молекулы. Структурная формула карбоната кальция имеет вид:
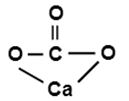
Карбонат кальция представляет собой среднюю соль угольной кислоты, которая способна диссоциировать на ионы в водном растворе согласно следующему уравнению:
CaCO3 ↔ Ca2+ + CO32-
В этой связи для карбоната кальция также можно указать и ионную формулу:
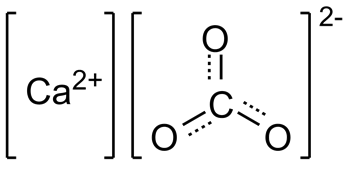
Примеры решения задач
| Задание | Образец соединения фосфора и брома массой 81,3 г содержит 0,3 моль фосфора. Найдите эмпирическую формулу соединения. |
| Решение | Рассчитаем массу фосфора в соединении (относительная атомная масса равна 31 а.е.м. и численно совпадает со значениями молекулярной и молярной масс):
m(P) = n(P) × M(P); m(P) = 0,3 × 31 = 9,3 г Определим массу брома в составе соединения: m(Br) = msubstance – m(P); m(Br) = 81,3 – 9,3 = 72 г Обозначим количество моль элементов, входящих в состав соединения за «х» (фосфор) и «у» (бром). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y = m(P)/Ar(P) : m(Br)/Ar(Br); x:y= 9,3/31 : 72/80; x:y= 0,3 : 0,9 = 1 : 3 Значит формула соединения фосфора и брома будет иметь вид PBr3. |
| Ответ | PBr3 |
| Задание | При нагревании некоторого вещества массой 1,225 г образовалось 0,745 г хлорида калия и выделился кислород объемом 0,336 л (н.у.). Найдите формулу соединения. |
| Решение | По массам хлорида калия и молекулярного кислорода находим количество вещества хлора, калия и кислорода. Однако, для начала рассчитаем молярные массы этих веществ. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr):
M(KCl) = Ar(K) + Ar(Cl) = 39+ 35,5 = 74,5 г/моль; M(O2) = 2×Ar(O) = 2×16= 32 г/моль KCl ↔ K+ + Cl—, значит, n(K) = n(Cl) и их массы также равны. n (K) = n(Cl) = m(KCl) / M(KCl); n (K) = n(Cl) = 0,74,5 / 74,5 = 0,01 моль n (O) = V(O2) / Vm×2; n (O) = 0,336 / 22,4 × 2 = 0,03 моль Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (хлор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом: x:y:z = n(K) : n(Cl) : n(O); x:y:z= 0,01 : 0,01 : 0,03 = 1 : 1 : 3 Следовательно, простейшая формула соединения калия, хлора и кислорода имеет вид KClO3. Это бертолетова соль. |
| Ответ | KClO3 |











