Формула металлического натрия
Определение и формула металлического натрия
Пар натрия имеет темно-красный цвет и состоит из атомов Na (преобладают) и молекул Na2.
Весьма реакционноспособный; на воздухе покрывается оксидной пленкой (тускнеет), воспламеняется приумеренном нагревании. Устойчив в атмосфере аргона и азота. Сильный восстановитель; энергично реагирует с водой, кислотами, неметаллами.
Хорошо сохраняется под слоем бензина или керосина, легко суспендируется в кипящих инертных растворителях (толуол, ксилол, гептан, октан и др.). В инертной атмосфере расплавленный натрий быстро распределяется по поверхности некоторых твердых веществ (NaCl, Na2СО3, уголь, железо, Аl2О3, ZrO2), образуя серо-черные моноатомные покрытия. Окрашивает пламя газовой горелки в желтый цвет.

Рис. 1. Металлический натрий. Внешний вид.
Химическая формула металлического натрия
Химическое обозначение натрия – Na от латинского слова «natrium». Этот химический элемент расположен в третьем периоде в IА группе Периодической таблицы Д.И. Менделеева. Относится к элементамs-семейства. Металл. Относительная атомная масса натрия равна 22,9898 а.е.м.
Электронная формула металлического натрия
В ядре атома натрия содержится 11 протонов и 12 нейтронов (массовое число равно 23). В атоме натрия есть три энергетических уровня, на которых находятся 11 электронов (рис. 2).
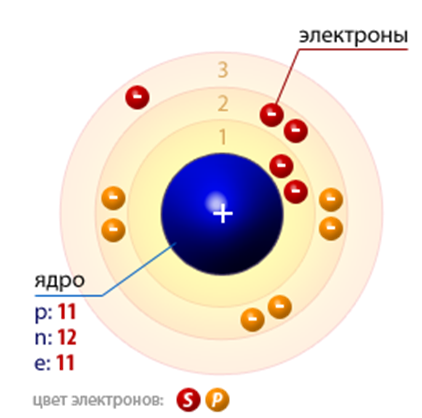
Рис. 2. Строение атома натрия.
Электронная формула атома натрия в основном состоянии имеет следующий вид:
+11Na)2)8)1;
1s22s22p63s1.
Примеры решения задач
| Задание | Определите молекулярную формулу кальциевой селитры, в которой массовые отношения кальция, азота и кислорода равны 10:7:24. Относительная молекулярная масса кальциевой селитры 164. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
n = m / M. Найдем молярные массы кальция, азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(N)=14 г/моль, а М(O) = 32 г/моль. Тогда, количество вещества этих элементов равно: n (Ca) = m (Ca) / M (Ca); n (Ca) = 10 / 40 = 0,25 моль. n (N) = m (N) / M (N); n (N) = 7 / 14 = 0, 5 моль. n (O) = m (O) / M (O); n (O) = 24 / 16 = 1,5 моль. Найдем мольное отношение: n(Ca) :n(N):n(O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6, т.е. простейшая формула соединения кальция, азота и кислорода имеет вид CaN2O6 и молярную массу 164 г/моль [M(CaN2O6) = Ar(Ca) + 2×Ar(N) + 6×Ar(O) = 40 + 2×14 + 6×16 = 40 + 28 + 96 = 164 г/моль] Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(CaN2O6) = 164 / 164 = 1. Значит формула соединения кальция, азота и кислорода имеет вид CaN2O6или Ca(NO3)2. Это нитрат кальция. |
| Ответ | Ca(NO3)2 |
| Задание | Установите массовую формулу вещества, содержащего 55,2% калия, 14,6% фосфора и 30,2% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(K)/Ar(K) : ω(P)/Ar(P) : ω(O)/Ar(O); x:y:z= 55,2/39 : 14,6/31 : 30,2/16; x:y:z= 1,4 : 0,5: 1,9 = 3 : 1: 4. Значит формула соединения калия, фосфора и кислорода будет иметь вид K3PO4. Это фосфат калия. |
| Ответ | K3PO4 |











