Формула красной кровяной соли
Определение и формула красной кровяной соли
Хорошо растворяется в воде, подвергается акватации и гидролизу по аниону CN—. На свету увеличивается степень гидролиза и ускоряется переход в гексацианоферрат (II) калия. Кристаллогидратов не образует. Не реагирует с разбавленными щелочами, гидратом аммиака. Разлагается кислотами. Окислитель. Вступает в реакции обмена.

Рис. 1. Красная кровяная соль. Внешний вид.
Химическая формула красной кровяной соли
Химическая формула красной кровяной соли K3[Fe(CN)6]. Она показывает, что в состав данной молекулы входят три атома калия (Ar = 39 а.е.м.), один атом железа (Ar = 56 а.е.м.), шесть атомов углерода (Ar = 12а.е.м.) и шесть атомов азота (Ar = 14 а.е.м.). По химической формуле можно вычислить молекулярную массу красной кровяной соли:
Mr(K3[Fe(CN)6]) = 3×Ar(K) + Ar(Fe) + 6×Ar(C) + 6×Ar(N);
Mr(K3[Fe(CN)6]) = 3×39 + 56 + 6×12 + 6×14 = 117 + 56 + 72 + 84 = 329.
Графическая (структурная) формула красной кровяной соли
Структурная (графическая) формула красной кровяной соли является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 2.).
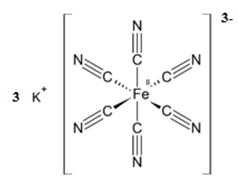
Рис. 2. Структурная формула красной кровяной соли.
Ионная формула
В водном растворе красная кровяная соль может диссоциировать согласно следующему уравнению:
K3[Fe(CN)6] ↔ 3K+ + [Fe(CN)6]3-;
[Fe(CN)6]3- ↔ Fe3+ + 6CN—.
Примеры решения задач
| Задание | При нейтрализации 25,5 г предельной одноосновной кислоты избытком раствора гидрокарбоната натрия выделилось 5,6 л (н.у.) газа. Определите молекулярную формулу кислоты. |
| Решение | Запишем уравнение реакции нейтрализации предельной одноосновной кислоты избытком раствора гидрокарбоната натрия в общем виде:
CnH2n+1COOH + NaHCO3 → CnH2n+1COONa + CO2↑ + H2O. Рассчитаем количество вещества выделившегося в ходе реакции углекислого газа: n = V / Vm; n(CO2) = V(CO2) / Vm; n(CO2) = 5,6 / 22,4 = 0,25 моль. Согласно уравнению реакции n(CO2): n(CnH2n+1COOH) = 1:1, т.е. n(CnH2n+1COOH) = n(CO2) = 0,25 моль. Рассчитаем молярную массу предельной одноосновной кислоты: M = m / n; M(CnH2n+1COOH) = m(CnH2n+1COOH) / n(CnH2n+1COOH); M(CnH2n+1COOH) = 25,5 / 0,25 = 102 г/моль. Определим число атомов углерода в молекуле предельной одноосновной кислоты (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: 12 – для углерода, 1 – для водорода и 16 для кислорода): M(CnH2n+1COOH) = 12n + 2n + 1 + 12 + 16 + 16 +1 = 14n + 46; 14n + 46 = 102 г/моль; 14n = 56; n = 4. Значит молекулярная формула предельной одноосновной кислоты C4H9COOH. |
| Ответ | C4H9COOH |
| Задание | Установите молекулярную формулу алкена, если известно, что 2,8 г его способны присоединить 1120 мл (н.у.) хлороводорода. |
| Решение | Запишем уравнение реакции присоединения хлороводорода к алкену в общем виде:
CnH2n + HCl → CnH2n+1Cl. Рассчитаем количество вещества хлороводорода: n = V / Vm; n(HCl) = V(HCl) / Vm; n(HCl) = 1,2 / 22,4 = 0,05 моль. Согласно уравнению реакции n(HCl): n(CnH2n) = 1:1, т.е. n(CnH2n) = n(HCl) = 0,05 моль. Рассчитаем молярную массу алкена: M = m / n; M(CnH2n) = m(CnH2n) / n(CnH2n); M(CnH2n) = 2,8 / 0,05 = 56 г/моль. Определим число атомов углерода в молекуле алкена (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: 12 – для углерода и 1 – для водорода): M(CnH2n) = 12n + 2n = 14n; 14n= 56 г/моль; n = 4. Значит молекулярная формула алкена C4H8. |
| Ответ | C4H8 |











