Формула карбонатов
Определение и формула карбонатов
Угольная кислота представляет собой двухосновную кислоту, которая подвергается ступенчатой диссоциации:
H2CO3 ↔ H+ + HCO3—;
HCO3— ↔ H+ + CO32-,
тем самым образуя соли – карбонаты – двух видов:
— карбонаты – замещены все атомы водорода в угольной кислоте, например, K2CO3 – карбонат калия, (NH4)2CO3 – карбонат аммония, CaCO3 — карбонат кальция;
— гидрокарбонаты – замещен один атом водорода в угольной кислоте, например, KHCO3 – гидрокарбонат калия, NH4HCO3 – гидрокарбонат аммония, Ca(HCO3)2 — гидрокарбонат кальция.
Химические формулы карбонатов
Химические формулы карбонатов рассмотрим на примере кальциевых солей угольной кислоты: CaCO3 — карбоната кальция и Ca(HCO3)2 — гидрокарбоната кальция. Химическая формула показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу карбонатов (Ar(Са) = 40 а.е.м., Ar(H) = 1 а.е.м., Ar(С) = 12 а.е.м., Ar(O) = 16 а.е.м.):
Mr(CaCO3) = Ar(Ca) + Ar(C) + 3×Ar(O);
Mr(CaCO3) = 40 + 12 + 3×16 = 52 +48 = 100.
Mr(Ca(HCO3)2) = Ar(Ca) + 2×Ar(H) + 2×Ar(C) + 6×Ar(O);
Mr(Ca(HCO3)2) = 40 + 2×1 +2×12 + 6×16 = 40 + 2 + 24 + 96 = 162.
Графическая (структурная) формула карбонатов
Структурная (графическая) формула является более наглядной. Рассмотрим структурные формулы карбонатов на примере все тех же кальциевых солей угольной кислоты: CaCO3 — карбоната кальция и Ca(HCO3)2 — гидрокарбоната кальция.
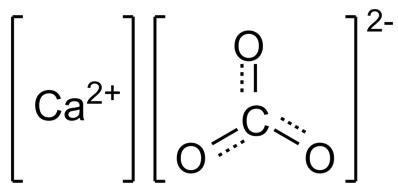
Рис. 1. Структурная формула карбоната кальция.
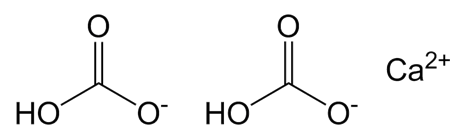
Рис. 2. Структурная формула гидрокарбоната кальция.
Ионная формула
Карбонаты представляют собой соли разного типа (средние и кислые), каждая из которых способна диссоциировать в водном растворе:
CaCO3 ↔ Ca2+ + CO32-;
Ca(HCO3)2 ↔ Ca2+ + 2HCO3—.
Примеры решения задач
| Задание | При полном сгорании 6 г органического вещества образовалось 8,8 г оксида углерода (IV) и 3,6 г воды. Определите молекулярную формулу сожженного вещества, если известно, что его молярная масса равна 180 г/моль. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz+ Oz→CO2 + H2O. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]×M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. Тогда, m(C) = [8,8 / 44]×12 = 2,4 г; m(H) = 2×3,6 / 18 ×1= 0,4 г. m(O) = m(CxHyOz) – m(C) – m(H) = 6 – 2,4 – 0,4 = 3,2 г. Определим химическую формулу соединения: x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O); x:y:z= 2,4/12 :0,4/1 :3,2/16; x:y:z= 0,2 : 0,4 : 0,2 = 1: 2 : 1. Значит простейшая формула соединения CH2O и молярную массу 30 г/моль [M(CH2O) = Ar(C) + 2×Ar(H) + Ar(O) = 12 + 2×1 + 16 = 12 + 2 + 16 = 30 / моль]. Чтобы найти истинную формулу органического соединения найдем отношение истинной и полученной молярных масс: Msubstance / M(CH2O) = 180 / 30 = 6. Значит индексы атомов углерода, водорода и кислорода должны быть в 6 раз выше, т.е. формула вещества будет иметь вид C6H12O6. Это глюкоза или фруктоза. |
| Ответ | C6H12O6 |
| Задание | Определите молекулярную формулу соли с молярной массой менее 300, в которой массовые доли азота, водорода, хрома и кислорода составляют 11,11%; 3,17%; 41,27% и 44,44% соответственно. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов азота в молекуле через «х», число атомов водорода через «у», число атомов хрома за «z» и число атомов кислорода за «k». Найдем соответствующие относительные атомные массы элементов железа и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(N) = 14; Ar(H) = 1; Ar(Cr) = 52; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y:z:k = m(N)/Ar(N) : m(H)/Ar(H) : m(Cr)/Ar(Cr) : m(O)/Ar(O); x:y:z:k= 11,11/14 :3,17/1 :41,27/52 : 44,44/16; x:y:z:k= 0,79 : 3,17 : 0,79 : 2,78 = 1: 4 : 1 : 3,5 = 2 : 8: 2 : 7. Значит простейшая формула соединения азота, водорода, хрома и кислорода имеет вид N2H8Cr2O7 или (NH4)2Cr2O7. Это дихромат аммония. |
| Ответ | (NH4)2Cr2O7 |











