Формула гидроксида
Определение и формула гидроксида
Основная классификация гидроксидов основывается на их природе. Различают основные, амфотерные и кислотные гидроксиды.
Основные гидроксиды (основания, щелочи)
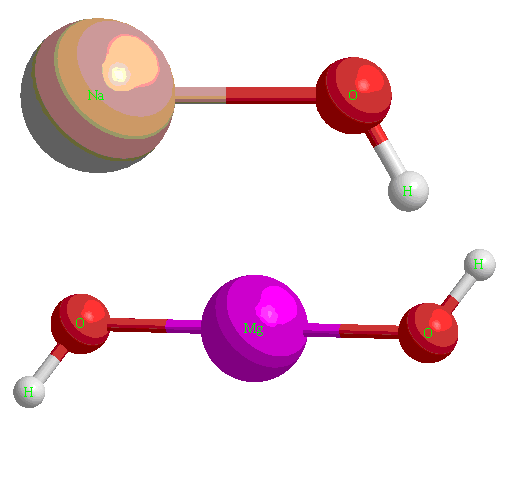
К ним относятся соединения металлов общей формулы ![]() или
или ![]() , а также раствор аммиака в воде (гидроксид аммония
, а также раствор аммиака в воде (гидроксид аммония ![]() ). В данных веществах металл принимает степень окисления или
). В данных веществах металл принимает степень окисления или ![]() или
или ![]() .
.
Примеры: ![]()
Щелочами называют гидроксиды щелочных и щелочно-земельных металлов, которые в воде они диссоциируют нацело, т.е. являются сильными электролитами.
Они проявляют типичные основные свойства реагируя с кислотными оксидами, кислотами, амфотерными соединениями (при сплавлении fus. и в растворе sol.), растворимыми солями:
![]()
![]()
![]()
![]()
![]()
Остальные основные гидроксиды обладают практически такими же химическими свойствами, но они как правило нерастворимы в воде и не взаимодействуют с амфотерными соединениями.
Амфотерные гидроксиды
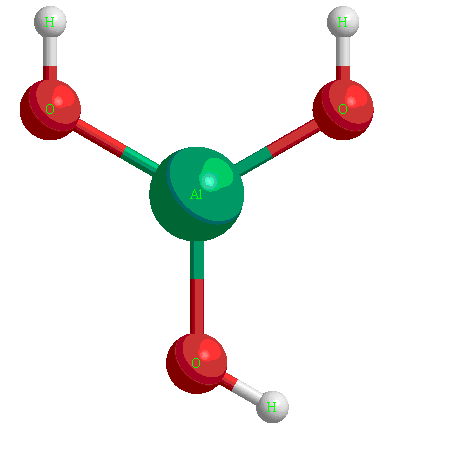
Это гидроксиды металлов со степенью окисления ![]() ,
, ![]() . Есть исключения (например,
. Есть исключения (например, ![]() ), в которых металл проявляет степень окисления
), в которых металл проявляет степень окисления ![]() .
.
Примеры: ![]() .
.
В зависимости от условий амфотерные вещества могут проявлять или основные или кислотные свойства.
Они представляют собой твёрдые вещества, которые не растворяются в воде, и так правило являются слабыми электролитами.
При воздействии температуры происходит разложение соединения с образованием амфотерного оксида, например:
![]()
При взаимодействии с кислотами образуются соли:
![]()
Пример реакции с сильным основанием в зависимости от условий проведения реакции рассмотрен выше.
Кислотные гидроксиды (кислородсодержащие кислоты)
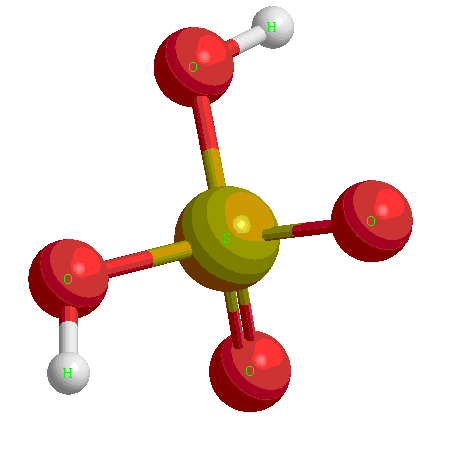
Это как правило гидроксиды неметаллов, имеющих степень окисления ![]() ,
, ![]() либо гидроксиды металлов в высших степенях окисления.
либо гидроксиды металлов в высших степенях окисления.
Примеры: ![]()
Большая часть неорганических кислот при обычных условиях находятся в жидком состоянии, некоторые – в твёрдом состоянии (ортофосфорная), а некоторые нельзя выделить в виде индивидуальных соединений.
Кислоты реагируют с основаниями, основными оксидами и металлами с образованием солей:
![]()
![]()
![]()
Примеры решения задач
| Задание | Сколько грамм орто-алюмината натрия можно получить из |
| Решение | Запишем уравнение химической реакции образования орто-алюмината натрия:
Найдем количество моль гидроксида алюминия, вступившего в реакцию: где Из стехиометрии реакции Найдем массу |
| Ответ | Масса орто-алюмината натрия равна |
| Задание | Определите во сколько раз растворимость гидроксида железа ( |
| Решение | Запишем уравнение равновесия малорастворимого соединения с его насыщенным раствором, в котором он диссоциирует нацело:
Запишем чему равно произведение растворимости (ПР) данного осадка: ПР= где Найдем чему равна растворимость Запишем уравнение равновесия гидроксида железа (III) с его насыщенным раствором, в котором он диссоциирует нацело: Покажем чему равно произведение растворимости уже этого осадка: ПР= где Найдем чему равна растворимость Теперь вычислим соотношение растворимостей осадков гидроксидов железа |
| Ответ | Растворимость гидроксида железа ( |











