Формула гидроксида меди 2
Определение и формула гидроксида меди 2
Термически неустойчивый. Не растворяется в воде. Переводится в раствор действием гидрата аммиака. Проявляет амфотерные свойства с преобладанием основных свойств; реагирует с разбавленными кислотами,концентрированными щелочами. Слабый окислитель и восстановитель.

Рис. 1. Свежеприготовленный гидроксид меди (II). Внешний вид.
Химическая формула гидроксида меди 2
Химическая формула гидроксида меди (II) Cu(OH)2. Она показывает, что в состав данной молекулы входят один атом меди (Ar = 64 а.е.м.), два атома водорода (Ar = 1 а.е.м.) и два атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу гидроксида меди (II):
Mr(Cu(OH)2) = Ar(Cu) + 2×Ar(H) + 2×Ar(O);
Mr(Cu(OH)2) = 64 + 2×1 + 2×16 = 64 + 2 + 32 = 98.
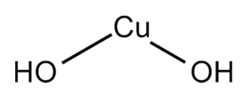
Графическая (структурная) формула гидроксида меди 2
Структурная (графическая) формула гидроксида меди (II) является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
Ионная формула
Гидроксид меди (II) представляет собой электролит, который диссоциирует на ионы в водном растворе согласно следующему уравнению реакции:
Cu(OH)2 ↔ Cu2+ + 2OH—.
Примеры решения задач
| Задание | При сжигании 26,7 г аминокислоты (CxHyOzNk) в избытке кислорода образуется 39,6 г оксида углерода (IV), 18,9 г воды и 4,2 г азота. Определите формулу аминокислоты. |
| Решение | Составим схему реакции сгорания аминокислоты обозначив количество атомов углерода, водорода, кислорода и азота за «x», «у», «z» и «k» соответственно:
CxHyOzNk+ Oz→CO2 + H2O + N2. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м., Ar(N) = 14 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]×M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. Тогда, m(C) = [39,6 / 44]×12 = 10,8 г; m(H) = 2×18,9 / 18 ×1= 2,1 г. m(O) = m(CxHyOzNk) – m(C) – m(H) – m(N)= 26,7 – 10,8 – 2,1 – 4,2 = 9,6 г. Определим химическую формулу аминокислоты: x:y:z:k = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O) : m(N)/Ar(N); x:y:z:k= 10,8/12 :2,1/1 :9,6/16 : 4,2/14; x:y:z:k= 0,9 : 2,1 : 0,41 : 0,3 = 3: 7 : 1,5 : 1 = 6 : 14: 3 : 2. Значит простейшая формула аминокислоты C6H14O3N2. |
| Ответ | C6H14O3N2 |
| Задание | Составьте простейшую формулу соединения, в котором массовые доли элементов приближенно равны: углерода – 25,4%, водорода – 3,17%, кислорода – 33,86%, хлора – 37,57%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов углерода в молекуле через «х», число атомов азота водорода через «у», число атомов кислорода за «z» и число атомов хлора за «k». Найдем соответствующие относительные атомные массы элементов углерода, водорода, кислорода и хлора (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(C) = 12; Ar(H) = 14; Ar(O) = 16; Ar(Cl) = 35,5. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y:z:k = ω(C)/Ar(C) : ω(H)/Ar(H) : ω(O)/Ar(O) : ω(Cl)/Ar(Cl); x:y:z:k= 25,4/12 : 3,17/1 : 33,86/16 : 37,57/35,5; x:y:z:k= 2,1 : 3,17 : 2,1 : 1,1 = 2 : 3 : 2 : 1. Значит простейшая формула соединения углерода, водорода, кислорода и хлора будет иметь вид C2H3O2Cl. |
| Ответ | C2H3O2Cl |











