Формула борной кислоты
Определение и формула борной кислоты
Растворяется в воде (растворимость сильно повышается с ростом температуры), проявляет слабые кислотные свойства. Реагирует со щелочами, концентрированной фтороводородной кислотой. Вступает в реакции комплексообразования.

Рис. 1. Борная кислота. Внешний вид.
Химическая формула борной кислоты
Химическая формула борной кислоты может быть записана двояко: H3BO3 или B(OH)3. Она показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу борной кислоты (Ar(B) = 11 а.е.м., Ar(Н) = 1 а.е.м., Ar(О) = 16 а.е.м.):
Mr(H3BO3) = 3×Ar(H) + Ar(B) + 3×Ar(О);
Mr(H3BO3) = 3×1 + 11 + 3×16 = 3 + 11 + 48 = 62.
Графическая (структурная) формула борной кислоты
Структурная (графическая) формула является более наглядной, она отражает то, как атомы связаны между собой внутри молекулы борной кислоты (рис. 2).
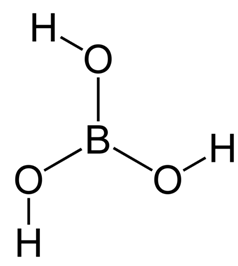
Рис. 2. Графическая формула борной кислоты.
Ионная формула
Борная кислота – слабый электролит. В водном растворе под действием электрического тока она частично диссоциирует на ионы согласно следующему уравнению:
H3BO3↔ 3H+ + BO33-.
Примеры решения задач
| Задание | При сжигании смеси, состоявшей из двух объемов неизвестного газа и полутора объемов кислорода, образовалась смесь из одного объема азота и трех объемов водяного пара. Во всех случаях объемы газов измерены при одинаковых условиях. Какова формула неизвестного газа? |
| Решение | Так как при сгорании неизвестного газа в кислороде образуются молекулярный азот (N2) и вода (H2O), то в состав газа входят азот, водород и, возможно, кислород. Обозначим количество атомов каждого из указанных химических элементов как «х», «у» и «z». Тогда формула неизвестного газа в общем виде будет записываться как NxHyOz.
Согласно закону объемных отношений, объемы газов пропорциональны их количествам вещества и равны коэффициентам в уравнении реакции. С учетом этого напишем уравнение реакции сгорании неизвестного газа в кислороде в общем виде: 2NxHyOz + 3/2 O2 = N2 + 3H2O. По закону сохранения массы веществ число атомов каждого элемента в левой и правой частях уравнения одинаково, поэтому 2х = 2; отсюда х = 1; 2у = 6; у = 3; 2z + 3 = 3; z = 0. Следовательно, формула неизвестного газа NH3. Это аммиак. |
| Ответ | NH3. Это аммиак |
| Задание | Выведите формулу кристаллогидрата фосфата цинка, если известно, что массовая доля соли в нем равна 84,2%. |
| Решение | Пусть в состав формульной единицы кристаллогидрата входит n молекул воды, т.е. формула данного кристаллогидрата Zn3(PO4)2×nH2O.
Рассчитаем молекулярную массу безводной соли: Mr(Zn3(PO4)2) = 3×Ar(Zn) + 2×Ar(P) + 8×Ar(O); Mr(Zn3(PO4)2) = 3×65 + 2×31 + 8×16 = 195 + 62 + 128 = 385. Известно, что M = Mr, значит M(Zn3(PO4)2) = 385 г/моль. Найдем молярную массу кристаллогидрата: ω(Zn3(PO4)2) = M(Zn3(PO4)2) / M(Zn3(PO4)2×nH2O)× 100%; M(Zn3(PO4)2×nH2O) = M(Zn3(PO4)2) × 100% /ω(Zn3(PO4)2); M(Zn3(PO4)2×nH2O) = 385 × 100% / 84,2 = 457 г/моль. Рассчитаем число молекул воды (молярная масса воды равна 18 г/моль): 457 = 385 + 18n; n = 4. Следовательно, формула кристаллогидрата фосфата цинка имеет вид Zn3(PO4)2×4H2O. |
| Ответ | Zn3(PO4)2×4H2O |











