Формула бертолетовой соли
Определение и формула бертолетовой соли
Температура плавления 357oC. Хорошо растворяется в воде (не гидролизуется). Кристаллогидратов не образует. Разлагается концентрированными кислотами. Сильный окислитель при спекании.

Рис. 1. Бертолетова соль. Внешний вид.
Химическая формула бертолетовой соли
Химическая формула бертолетовой соли KClO3. Она показывает, что в составе молекулы этого вещества находится один атом калия (Ar = 39 а.е.м.), один атом хлора (Ar = 35,5 а.е.м.) и три атома кислорода (Ar = 35,5 а.е.м.). По химической формуле можно вычислить молекулярную массу бертолетовой соли:
Mr(KClO3) = Ar(K) + Ar(Cl) + 3×Ar(O);
Mr(KClO3) = 39 + 35,5 + 3×16 = 74,5 + 48 = 122,5.
Структурная (графическая) формула бертолетовой соли
Структурная (графическая) формула бертолетовой соли является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы:
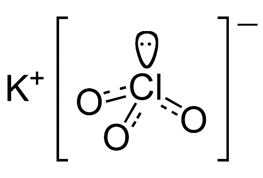
Ионная формула
Бертолетова соль является электролитом, т.е. в водном растворе диссоциирует на ионы согласно следующему уравнению:
KClO3 ↔ K+ + ClO3—.
Примеры решения задач
| Задание | В состав вещества входят 30,7% калия, 25,2% серы, 44% кислорода. Вывести формулу этого соединения. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов калия в молекуле через «х», число атомов серы через «у» и число атомов кислорода через «z». Найдем соответствующие относительные атомные массы элементов калия, серы и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(K) = 39; Ar(S) = 32; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y:z = ω(K)/Ar(K) : ω(S)/Ar(S) : ω(O)/Ar(O); x:y:z= 30,7/39 : 25,2/32 : 44/16; x:y:z= 0,787 : 0,787 : 2,75. Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,787): 0,787/0,787 : 0,787/0,787 : 2,75/0,787; 1 : 1: 3,5 = 2 : 2: 7. Следовательно, простейшая формула соединения калия, серы и кислорода имеет вид K2S2O7. |
| Ответ | K2S2O7 |
| Задание | При сжигании 8,4 г углеводорода получили 26,4 г углекислого газа и 10,8 г воды. Относительная плотность паров углеводорода по воздуху равна 42. Найдите молекулярную формулу углеводорода. |
| Решение | Значение молярной массы углеводорода можно определить при помощи его плотности по водороду:
M (CxHy) = M(H2) × D(H2); M (CxHy) = 2 × 42 = 84 г/моль. По массам углекислого газа и воды находим массы углерода и водорода. Однако, для начала рассчитаем их молярные массы. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. m (C) = m(CO2) × Ar(C)/M(CO2); m (C) = 26,4×12/44 = 7,2 г. m (H) = m(H2O) ×2×Ar(H)/M(H2O); m (H) = 10,8 × 2×1 / 18 = 1,2 г. Обозначим количество моль элементов, входящих в состав соединения за «х» (углерод) и «у» (водород). Тогда, мольное отношение будет выглядеть следующим образом: x:y = m(C)/Ar(C) : m(H)/Ar(H); x:y= 7,2/12 : 1,2/1; x:y= 0,6 : 1,2 = 1 : 2. Следовательно, простейшая формула углеводорода имеет вид CH2и молярную массу 14 г/моль [M(CH2) = Ar(C) + 2×Ar(H) = 12+ 2×1 = 12 + 2 = 14 г/моль]. Чтобы найти истинную формулу оксида хлора найдем отношение полученных молярных масс: M (CxHy) / M(CH2) = 84 / 14 = 6. Значит индексы атомов углерода и водорода должны быть в 6 раз выше, т.е. формула углеводорода будет иметь вид C6H12. Это гексен. |
| Ответ | C6H12 |











