Формула бензола
Определение и формула бензола
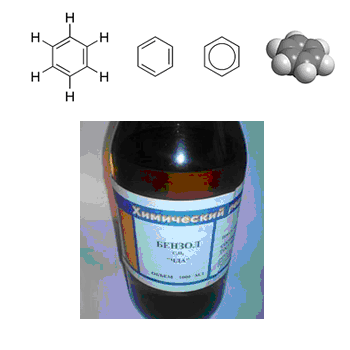
Химическая формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – в обычных условиях представляет собой бесцветную жидкость с определенным резким запахом.
Химические свойства бензола
- Для бензола типичными являются реакции электрофильного замещения в кольцо. Он реагирует с непредельными углеводородами, галогеналканами, галогенами, сильными кислотами. Реакции расщепления ароматического кольца проходят в жёстких условиях.
![Rendered by QuickLaTeX.com \[ C_6H_6 + Cl_2 \xrightarrow[]{FeCl_3} C_6H_5Cl + HCl \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-8c08b8b32281e0850d33f2564d5ffdf6_l3.png)
![Rendered by QuickLaTeX.com \[ C_6H_6 + 3Cl_2 \xrightarrow[]{T, h\nu} C_6H_6Cl_6 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-e90974cb3694a39603cef3c51af572f7_l3.png)
![Rendered by QuickLaTeX.com \[ C_6H_6 + C_2H_5Br \xrightarrow[]{FeBr_3} C_6H_5C_2H_5 + HBr \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-17bfe241fc8456616342de6e4b2da077_l3.png)
![Rendered by QuickLaTeX.com \[ C_6H_6 + HNO_3 \xrightarrow[]{H_2SO_4} C_6H_5NO_2 + H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-82765b72b87b43dc601dde8eb49c2ce5_l3.png)
![Rendered by QuickLaTeX.com \[ C_6H_6 + H_2SO_4 \rightarrow C_6H_5SO_3H + H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-d1d8fec589c697342060de46ee6d2907_l3.png)
Применение
Бензол в основном применяют для синтеза других органических веществ, а именно: этилбензола, кумола, циклогексана, нитробензола.
Примеры решения задач
| Задание | Какой объём водорода присоединится к |
| Решение | При гидрировании бензола исчезает ароматический характер ядра. Запишем уравнение реакции гидрирования бензола, в ходе которой образуется циклогексан:
Определим количество вещества бензола: По уравнению реакции гидрирования вычислим количество водорода, который присоединяется к бензолу: Откуда: По формуле, устанавливающей связь между химическим количеством вещества и объемом, рассчитаем объем водорода, который затрачен на гидрирование бензола: Получаем: |
| Ответ | |
| Задание | Если выход бензола |
| Решение | Запишем уравнение химической реакции получения бензола путем тримеризации ацетилена – реакция Зелинского:
Запишем формулу для определения выхода продукта: Определим количество моль ацетилена: По уравнению реакции определим теоретическое количество бензола: из из Тогда: Рассчитаем теоретическую массу образующегося бензола: Рассчитаем практическую массу получения бензола по формуле: |
| Ответ |











