Формула азотистой кислоты
Определение и формула азотистой кислоты
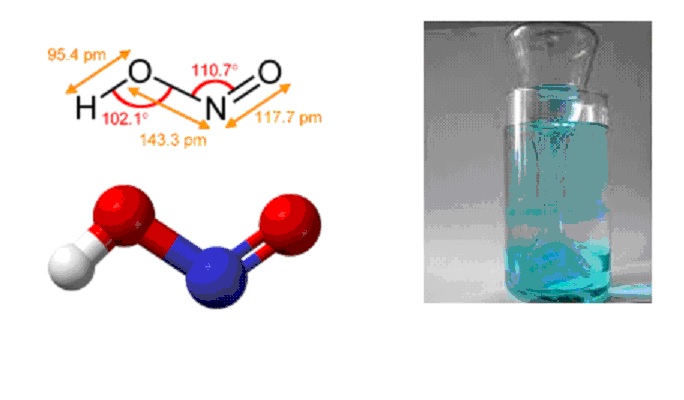
Химическая формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – существует в виде водного разбавленного раствора, который имеет слабый голубой оттенок, или в газовой фазе.
Химические свойства азотистой кислоты
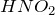 — одноосновная слабая кислота. В водных растворах подвергается электролитической диссоциации в одну стадию. Её показатель константы диссоциации равен
— одноосновная слабая кислота. В водных растворах подвергается электролитической диссоциации в одну стадию. Её показатель константы диссоциации равен 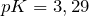 .
.
-
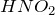 взаимодействует со щелочами, с окислителями и восстановителями:
взаимодействует со щелочами, с окислителями и восстановителями:
![Rendered by QuickLaTeX.com \[ HNO_2 + NaOH = NaNO_2 + H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-57bde9ddea31199cda3a94e3529b5664_l3.png)
![Rendered by QuickLaTeX.com \[ 2HNO_2 + O_2 = 2HNO_3 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-a87ae5c3c8e9599675845266603f37d6_l3.png)
![Rendered by QuickLaTeX.com \[ HNO_2 + H_2O_2 = HNO_3 + H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-13af30c6e2a80cb83c716ec9c8e220e4_l3.png)
![Rendered by QuickLaTeX.com \[ 2HNO_2 + 2HI = I_2 + 2NO \uparrow + 2H_2O \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-02fc8755009c6efa5e7be4d49c1f896b_l3.png)
Получение азотистой кислоты
Азотистая кислота образуется при взаимодействии оксида азота (III) ![]() с водой:
с водой:
![]()
Также её можно получить при взаимодействии сильных неорганических кислот с нитритами:
![]()
Применение
Азотистая кислота используется при диазотирования первичных ароматических аминов и синтезе солей диазония.
Качественная реакция
Качественной реакцией на азотистую кислоту является образование тёмно-бурого раствора сульфата нитрозожелеза (II) при взаимодействии ![]() с
с ![]() в слабо кислой среде:
в слабо кислой среде:
![]()
![]()
Примеры решения задач
| Задание | Рассчитайте эквивалентную электрическую проводимсоть раствора с концентрацией |
| Решение | Запишем уравнение закона разбавления Оствальда:
Вычислим Рассчитаем |
| Ответ |
| Задание | На основании первой задачи рассчитайте удельную электропроводность раствора. |
| Решение | Запишем выражение для удельной электропроводности Определим фактор эквивалентности Рассчитаем нормальность Найдем |
| Ответ | |











