Формула аренов
Определение и общая формула аренов
Общая формула гомологического ряда бензола CnH2n-6. Простейшими представителями ароматических углеводородов являются бензол – C6H6 и толуол – C6H5-CH3. Углеводородные радикалы, полученные из аренов носят названия: C6H5 – — фенил (Ph-) и C6H5-CH2— — бензил.
Первые члены гомологического ряда бензола – бесцветные жидкости со специфическим запахом. Они легче воды и в ней практически нерастворимы. Хорошо растворяются в органических растворителях и сами являются хорошими растворителями.
Рассмотрим подробнее на примере толуола, ближайшего гомолога бензола.
Химическая формула аренов
Химическая формула толуола C6H5CH3. Она показывает, что в состав данной молекулы входят семь атомов углерода (Ar = 12 а.е.м.) и восемь атомов водорода (Ar = 1 а.е.м.). По химической формуле можно вычислить молекулярную массу толуола:
Mr(C6H5CH3) = 7×Ar(C) + 8×Ar(H);
Mr(C6H5CH3) = 7×12 + 8×1 = 84 + 8 = 92.
Графическая (структурная) формула аренов
Структурная (графическая) формула толуола является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 1).
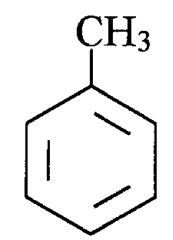
Рис. 1. Структурная формула толуола.
Примеры решения задач
| Задание | При полном сгорании 6 г органического вещества образовалось 8,8 г оксида углерода (IV) и 3,6 г воды. Определите молекулярную формулу сожженного вещества, если известно, что его молярная масса равна 180 г/моль. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
CxHyOz+ Oz→CO2 + H2O. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO2)×M(C) = [m(CO2) / M(CO2)]×M(C); m(H) = n(H)×M(H) = 2×n(H2O)×M(H) = [2×m(H2O) / M(H2O)]×M(H); Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H2O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. Тогда, m(C) = [8,8 / 44]×12 = 2,4 г; m(H) = 2×3,6 / 18 ×1= 0,4 г. m(O) = m(CxHyOz) – m(C) – m(H) = 6 – 2,4 – 0,4 = 3,2 г. Определим химическую формулу соединения: x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O); x:y:z= 2,4/12 :0,4/1 :3,2/16; x:y:z= 0,2 : 0,4 : 0,2 = 1: 2 : 1. Значит простейшая формула соединения CH2Oи молярную массу 30 г/моль [M(CH2O) = Ar(C) + 2×Ar(H) + Ar(O) = 12 + 2×1 + 16 = 12 + 2 + 16 = 30 / моль]. Чтобы найти истинную формулу органического соединения найдем отношение истинной и полученной молярных масс: Msubstance / M(CH2O) = 180 / 30 = 6. Значит индексы атомов углерода, водорода и кислорода должны быть в 6 раз выше, т.е. формула вещества будет иметь вид C6H12O6. Это глюкоза или фруктоза. |
| Ответ | C6H12O6 |
| Задание | Выведите простейшую формулу соединения, в котором массовая доля фосфора составляет 43,66%, а массовая доля кислорода – 56,34%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов фосфора в молекуле через «х», а число атомов кислорода через «у» Найдем соответствующие относительные атомные массы элементов фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(P) = 31; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y = ω(P)/Ar(P) : ω (O)/Ar(O); x:y = 43,66/31 : 56,34/16; x:y: = 1,4 : 3,5 = 1 : 2,5 = 2 : 5. Значит простейшая формула соединения фосфора и кислорода имеет вид P2O5. Это оксид фосфора (V). |
| Ответ | P2O5 |











