Формула алмаза
Определение и формула алмаза

Химическая формула – ![]()
Молярная масса равна ![]() г/моль.
г/моль.
Физические свойства – это одно из самых твёрдых веществ с плотностью 3,47—3,55 г/см![]() , обычно бесцветный, но может иметь различные цвета, прозрачный, хрупкий, блестящий.
, обычно бесцветный, но может иметь различные цвета, прозрачный, хрупкий, блестящий.
Плохо проводит электрический ток. Не плавится, сублимируется при ![]() , устойчив при нагревании в отсутствие кислорода.
, устойчив при нагревании в отсутствие кислорода.
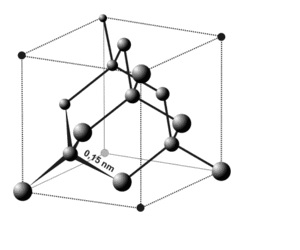
Кристаллическая решетка алмаза гранецентрированная кубическая (а = 0,357 нм, z = 4). Атомы углерода в алмазе имеют ![]() -гибридизацию. Каждый атом С в структуре алмаза находится в центре тетраэдра, вершинами которого служат четыре соседних атома.
-гибридизацию. Каждый атом С в структуре алмаза находится в центре тетраэдра, вершинами которого служат четыре соседних атома.
На рисунке ниже показана элементарная ячейка алмаза:
Химические свойства алмаза
- Так как алмаз очень твёрдое вещество, то он является достаточно инертным, поэтому его основная реакция – это горение в кислороде при высокой температуре:
![Rendered by QuickLaTeX.com \[ 2C + O_2 = 2CO \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-2f6ce8ddb9640ecf66956b5df946eb92_l3.png)
![Rendered by QuickLaTeX.com \[ C + O_2 = CO_2 \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-6f8340c9b97f2e0f40a09bc3f66effb3_l3.png)
Получение алмаза
Алмаз является природным ископаемым, хотя его можно получить и искусственно. В промышленности алмазы получают из графита при высоких температуре и давлении.
Применение
Алмаз используется для создания ювелирных украшений, для изготовления ножей, свёрл, резцов, применяется как абразив, используется в микроэлектронике.
Примеры решения задач
| Задание | Рассчитайте константу равновесия превращения алмаза в графит при |
| Решение | Запишем уравнение реакции:
Рассчитаем изменение энтальпии и энтропии реакции: Рассчитаем изменение энергии Гиббса реакции: Рассчитаем константу равновесия: |
| Ответ | |
| Задание | Рассчитайте изменение теплоемкости при превращении алмаза в графит при |
| Решение | Запишем уравнение реакции:
Рассчитаем изменение теплоемкости: |
| Ответ |











