Формула ацетатов
Определение и формула ацетатов
Уксусная кислота представляет собой одноосновную кислоту, которая подвергается диссоциации в водном растворе согласно следующему уравнению:
CH3COOH ↔ H+ + CH3COO—.
тем самым образуя соли – ацетаты (CH3COO)Na – ацетат натрия, (CH3COO)2Ca – ацетат кальция, (CH3COO)3Al–ацетат алюминия и т.д.).
В обычных условиях ацетаты представляют собой твердые вещества кристаллической природы, хорошо растворимые в воде.
Химическая формула ацетатов
Химические формулы ацетатов рассмотрим на примере CH3COONa – ацетата натрия, (CH3COO)2Ca – ацетата кальция, (CH3COO)3Al –ацетата алюминия. Химическая формула показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу хлоридов (Ar(Na) = 23а.е.м., Ar(C) = 12 а.е.м., Ar(Ca) = 40 а.е.м., Ar(Al) = 27а.е.м., Ar(O) = 16 а.е.м., Ar(H) = 1 а.е.м.):
Mr(CH3COONa) = Ar(Na) + 2×Ar(C)+ 3×Ar(H)+ 2×Ar(O);
Mr(CH3COONa) = 23 + 2×12 + 3×1 + 2×16 = 23 + 24 + 3 + 32 = 82.
Mr((CH3COO)2Ca) = Ar(Ca) + 4×Ar(C) + 6×Ar(H) + 4×Ar(O);
Mr((CH3COO)2Ca) = 40 + 4×12 + 6×1 + 4×16 = 40 + 48 + 6 + 64 = 158.
Mr(CH3COO)3Al) = Ar(Al) + 6×Ar(C) + 9×Ar(H) + 6×Ar(O);
Mr(CH3COO)3Al) = 27 + 6×12+ 9×1 + 6×16= 27 + 72 + 9 + 96 = 204.
Графическая (структурная) формула ацетатов
Структурная (графическая) формула является более наглядной. Рассмотрим структурные формулы ацетатов на примере все тех же CH3COONa – ацетата натрия, (CH3COO)2Ca – ацетата кальция, (CH3COO)3Al –ацетата алюминия.
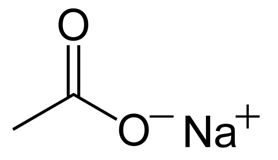
Рис. 1. Структурная формула ацетата натрия.
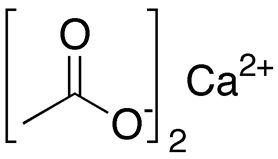
Рис. 2. Структурная формула ацетата кальция.
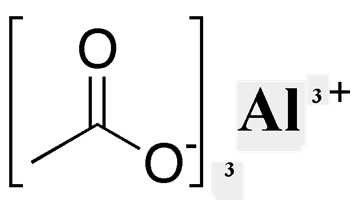
Рис. 3. Структурная формула ацетата алюминия.
Ионная формула
Ацетаты представляют собой средние соли способные диссоциировать на ионы в водном растворе:
CH3COONa ↔ Na+ + CH3COO—;
(CH3COO)2Ca↔ Ca2+ + 2CH3COO—;
(CH3COO)3Al↔ Al3+ + 3CH3COO—.
Примеры решения задач
| Задание | Массовая доля фосфора в одном из его оксидов равна 56,4%. Плотность паров оксида по воздуху равна 7,59. Установите молекулярную формулу оксида. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Вычислим массовую долю кислорода в соединении: ω (O) = 100% — ω(P) = 100% — 56,4% = 43,6%. Обозначим количество моль элементов, входящих в состав соединения за «х» (фосфор), «у» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y = ω(P)/Ar(P) : ω(O)/Ar(O); x:y= 56,4/31 : 43,6/16; x:y= 1,82 : 2,725= 1 : 1,5 = 2 : 3. Значит простейшая формула соединения фосфора с кислородом будет иметь вид P2O3 и молярную массу 94 г/моль [M(P2O3) = 2×Ar(P) + 3×Ar(O) = 2×31+ 3×16 = 62 + 32 = 94 г/моль]. Значение молярной массы органического вещества можно определить при помощи его плотности по воздуху: Msubstance = Mair × Dair; Msubstance = 29 × 7,59 = 220 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(P2O3) = 220 / 94 = 2. Значит индексы атомов фосфора и кислорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид P4O6. |
| Ответ | P4O6 |
| Задание | Определите молекулярную формулу соединения, содержащего 49,4% калия, 20,2% серы, 30,4% кислорода, если относительная молекулярная масса этого соединения в 3,95 раза больше относительной атомной массы кальция. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (сера) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(K)/Ar(K) : ω(S)/Ar(S) : ω(O)/Ar(O); x:y:z= 49,4/39 : 20,2/32 : 30,4/16; x:y:z= 1,3 : 0,63:1,9 = 2 : 1: 3. Значит простейшая формула соединения калия, серы и кислорода будет иметь вид K2SO3 и молярную массу 158 г/моль[M(K2SO3) = 2×Ar(K) + Ar(S) + 3×Ar(O) = 2×39 + 32 + 3×16 = 78 + 32 + 48 = 158 г/моль]. Найдем истинную молярную массу этого соединения: Msubstance = Ar(Ca) × 3,95 = 40 × 3,95 = 158 г/моль. Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс: Msubstance / M(K2SO3) = 158 / 158 = 1. Значит формула соединения калия, серы и кислорода имеет вид K2SO3. |
| Ответ | K2SO3 |











